
11.A、B两相同容器内均进行如下反应 ( )
CO(g)+H2(g) CO2(g)+H2(g) △H=-43 kJ·mol-1
CO2(g)+H2(g) △H=-43 kJ·mol-1
下列有关说法正确的是 ( )
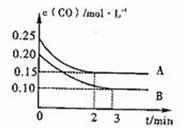
A.由图象可知,B容器内反应速率较快
B.前2min内,A容器中V(CO)=1.5 mol·L-1·min-1
C.若容器体积为10L,则3min内,B容器中反应放出热量43kJ
D.将A、B容器体积均压缩至原来的一半,则两容器内平衡均向右移动
10.
 下列说法中正确的是 ( )
下列说法中正确的是 ( )
A.SO2(g)+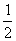 O2(g)
O2(g) SO3(g);△H=-98.3kJ·mol-1,当1 mol SO2与0.5 mol O2充分反应生成SO3时,放出热量98.3kJ。
SO3(g);△H=-98.3kJ·mol-1,当1 mol SO2与0.5 mol O2充分反应生成SO3时,放出热量98.3kJ。
B.3SO2(g)+O2(g) 2SO3(g);△H1>△H(△H数据A选项给出)
2SO3(g);△H1>△H(△H数据A选项给出)
C.X(g)+Y(g)  Z(g)+W(g);△H>0平衡后加入适量X,则
Z(g)+W(g);△H>0平衡后加入适量X,则 增大
增大
D.X(g)+Y(g) Z(g)+W(g);△H<0,平衡后加入适量X,则放出热量增加
Z(g)+W(g);△H<0,平衡后加入适量X,则放出热量增加
9.
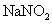 是一种食品添加剂,具有致癌作用。酸性
是一种食品添加剂,具有致癌作用。酸性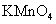 溶液与
溶液与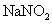 的反应为:
的反应为:
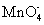 +
+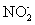 +
+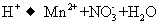 (未配平)。下列叙述正确的是 ( )
(未配平)。下列叙述正确的是 ( )
A.反应中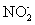 是氧化剂
是氧化剂
B.反应过程中溶液pH减小
C.1mol KMnO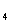 可以消耗2.5
可以消耗2.5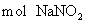
D.该反应可说明氧化性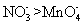
8.下列有关化学事实或现象解释正确的是 ( )
A.加热煮沸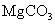 悬浊液,最终得到
悬浊液,最终得到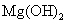 沉淀,说明
沉淀,说明
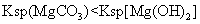
B.用丁达尔效应区分澄清透明的淀粉溶液和饱和食盐水
C.电解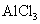 水溶液,阴极周围出现白色胶状沉淀,说明
水溶液,阴极周围出现白色胶状沉淀,说明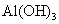 胶体粒子带正电荷
胶体粒子带正电荷
D.气体甲通入溶液乙,溶液乙颜色褪去,说明气体甲一定有漂白性
7.下列说法正确的是 ( )
A.能发生银镜反应的有机物都属于醛类
B.苯酚沾在皮肤上应立即用浓NaOH溶液冲洗
C.烃基跟羟基直接相连的有机物都属于醇类
D.皂化反应在碱性条件下进行
33.(8分)[化学一有机化学基础]
有机物X是某一感光树脂的单体,其结构式为
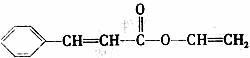
(1)由有机物X的结构推测,X能发生的反应有 。(填序号)。
A.能使溴的四氯化碳溶液退色
B.能使酸性高锰酸钾溶液退色
C.能与银氨溶液发生银镜反应
D能与NaHcO3溶液反应放出CO2
一定条件下,合成有机物X时,发生下列反应:
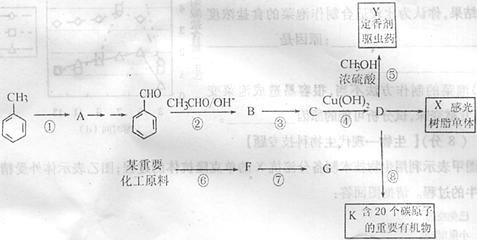
提示:a.由质谱图表明,G的相对分子质量为62;红外光谱表明,分子中含有碳氧单键核磁共振谱表明。分子中由2种类型的氢原子。
b.
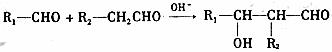
依据上述反应流程和有关提示,回答下列问题:
(2)上述反应中,B到C发生 (填反应类型)。
(3)写出K的结构简式 。(填反应类型)。
(4)写出反应⑤的化学方程式 。
(5)写出2种与化合物C具有相同官能团(不包括c)的芳香族化合物的结构简式 。
32.(8分)[化学一物质结构与性质]
A、B、M、X、Y、Z是元素周期表中的前20号元素.且原子序数依次增大。已知它们的部分化合物的性质如下表所示:
|
A的最简氢化物 |
B的最简氢化物 |
M的最简氢化物 |
X的氧化物 |
Y的最简氢化物 |
Z的最高价气氧化物 |
|
含氢量最高的有机物 |
水溶液呈碱性 |
水溶液呈碱性 |
两性氧化物 |
分子呈正四面体构型 |
对应水化物为最强酸 |
回答下列问题
(1)写出X原子的电子排布式 。
(2)A、B、M电负性由大到小的排列顺序为 。
(3)Y的最简氢化物中,Y原子的杂化形式是 。
(4)B的最简氢化物分子的空间构型是 ,属于 分子(填“极性”或“非极性”)。
(5)比较熔点高低:A最高价氧化物的熔点 Y最高价氧化物的熔点。
(6)判断沸点高低:M氢化物的拂点 Z氢化物的沸点,原因是 。
31.(8分)[化学一化学与技术]
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下:
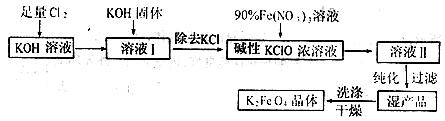
已知:
①2KOH+C12→KC1+KCO+H2O(条件:温度较低)
②6KOH+3C12→5KC1+KC1O3+3H2O(条件:温度较高)
回答下列问题:
(1)该生产工艺应在 (填“温度较高”或“温度较低”)的情况下进行。
(2)在“溶液I”中加KOH固体的目的是 (填序号)。
A.与“溶液I”中过量的C12继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供反应物
D.使副产物KClO3转化为KClO
(3)K2FeO4,具有强氧化性的原因 ;
(4)K2FeO4消毒后的还原产物具有净水作用,试解释其净水原理 。
(5)写出生成“溶液Ⅱ”的化学方程式 。
30.(17分)某研究性学习小组的同学为检测用H2还原CuO所得红色固体中是否含有Cu2O(红色),进行了认真的探究活动。他们通过查阅资料,获得如下信息.①Cu2O属于碱性氧化物;②Cu2O在酸性条件下发生Cu2O+2H+=Cu+Cu2++H2O反应;③高温灼烧CuO生成Cu2O和O2。
学习小组甲的同学们设计了如下实验方案:
[方案1]取该红色样品溶于足量的稀硝酸中,观察溶液颜色变化;
[方案2]取该红色样品溶于足量的稀硫酸中,观察溶液颜色变化;
[方案3]称取干燥坩埚的质量为a g,取红色固体置于坩埚中称得总质量为b g,在空气中高温灼烧至质量恒定,称得最后总质量为c g。
(1)你认为上述方案中不能达到设计目的的是 ,理由是 。
(2)若红色固体中含有CuO2,则a、b、c符合的数学关系式为 。
学习小组乙的同学们设计了另外的探究方案,即
[方案4],装置如下图所示,拟通过干燥管中无水硫酸铜是否变蓝来判断样品中是否含有Cu2O。
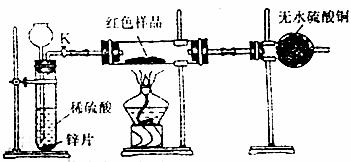
(3)简述该探究方案中。检验气体发生装置气密性的方法 。
(4)为确保探究的科学、合理、安全,实验中还应采取的措施有(你认为有几条,就回答几条):
① ;
② ;
③
④
学习小组丙的同学,用足量的铜与适量一定浓度的浓硝酸反应来测定NO2气体和NO气体的物质的量之比(用m表示)。请从下图中选用适当的装置,帮助丙组同学设计一个合理而简单的实验,用于测定m的值。E装入适量的水,供量气用,乙管可上下移动,用来调节液面高低。
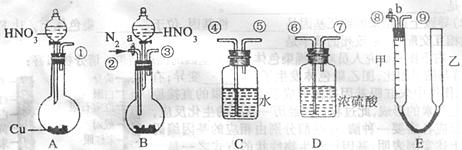
(5)实验中,应选择 (填序号)作为气体发生装置,理由是 。
(6)简单实验装置的连接顺序是(填各装置接口的编号) 。
(7)要测定m值,需要的实验数据有 。
[选做部分]
29.(12分)把大气中游离态的氮转化为氮的化合物的过程称为固氮。生物固氮和大气固氮(闪电时N2转化为NO)属于自然固氮,这远不能满足人类的需要。工业固氮(合成氮)是目前人工固氮的主要方法。有关大气固氮和工业固氮的平衡常数K值分别如下表一和表二。
表一:N2+O2  2NO 表二:N2+3H2
2NO 表二:N2+3H2  2NH3
2NH3
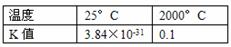
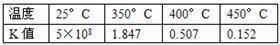
(1)根据上表中的数据分析,下列说法正确的是 (填序号)。
A.在常温下,大气固氮几乎不可能,而工业固氮反应程度大,由于反应太慢仍不可取
B.大气固氮与工业固氮都是放热反应
C.在常温下,大气固氮与工业固氮完成程度相关很大
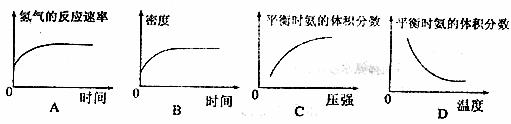
(2)在一定条件下,工业固氮在一固定体积的密闭容器中进行直至平衡,有人画出了下列图像A和B;达到平衡后,向密闭容器中分别充入稀有气体使压强增大或升高温度,有人又分别画出了如下图像C和D。其中有关图像正确的是 (填序号)。
(3)已知拆开1molH-H键、1molN-H键、1molN=N键分别是需要的能量是436kJ、391kJ、945.6kJ,则N2与H2反应生成的NH3的热化学方程式为 。
(4)合成氮工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:
N2(g)+3H2(g) 2NH3(g),673k,
2NH3(g),673k,
30Mpa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是
(填序号)。
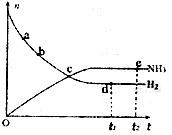
A.点a的正反应速率比点b的大
B.点c处反应达到平衡
C.点d(t1时刻)和点e(t2时刻)处n(N2)不一样
D.其他条件不变,773K下反应至t1时刻,n(H2)比上图中d点值大
(5)1998年希腊亚里多德大学的Marnellos和Stoukides采用高质子导电性的SCY陶瓷(能传递H+),实现了一定条件下高转化率的电化学合成氨。其实验装置如图。
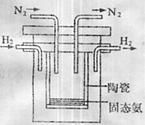
阴极的电极反应式为 。
(6)Ag+可与过量氨水反应生成[Ag(NH3)2]+,请解释为什么难溶于水和稀硝酸的氯化银却能溶于氨水中?请配以必要的方程式和文字来解释 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com