
31ЃЎ(8Зж)[ЛЏбЇ--ЛЏбЇгыММЪѕ]
КЃЫЎжаУОЕФзмДЂСПдМЮЊ2.1ЁС15tЃЌФПЧАЪРНчЩЯЕФ60%ЕФУОРДздКЃЫЎЁЃЙЄвЕЙцФЃКЃЫЎЬсУОЁЁ ЕФСїГЬШчЭМЫљЪОЃК
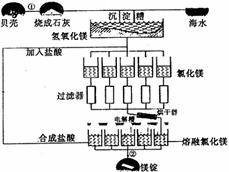
ЁЁЁЁЁЁ ЪдЛиД№ЯТСаЮЪЬтЃК
ЁЁ (1)ЧыаДГіКЃЫЎЬсУОЕФЙ§ГЬжаЂйЂкЗДгІЕФЛЏбЇЗНГЬЪНЃКЂйЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
ЁЁЁЁЁЁЁЁ ЂкЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЃ
ЁЁ (2)ЙЄвЕЩЯВЩгУЕчНтMgCl2ЕФЗНЗЈжЦЕУН№ЪєУОЃЌЕчНтВлжавѕМЋЕФЕчМЋЗДгІЪНЮЊЃК
ЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(3)ЙЄвЕЩЯжЦШЁН№ЪєТСЪБВЛгУЕчНтAlCl3ЕФЗНЗЈЖјЪЧгУЕчНтШлШкAl2O3ЕФЗНЗЈЃЌЪдНтЪЭТСЕчНтВлжаЕФбєМЋЬМПщЮЊКЮвЊЖЈЦкИќЛЛЃПЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЃ
30ЃЎ(14Зж)
ЭљЭбжЌУоАќЙќЕФМзЮяжЪжаЕЮШыЩйСПЫЎЃЌПЩЪЙУоЛЈзХЛ№ШМЩеЃЛБћЪЧФГживЊПѓЮяЕФжївЊГЩЗжЃЌЫќгЩСНжждЊЫизщГЩЃЌЦфдзгИіЪ§БШЮЊlЃК2ЃЌJЪЧвЛжжЧПЫсЃЌGгыJЗДгІЃЌЫљЕУШмвКГЪЛЦЩЋЃЛCЪЧЦјЬхЁЃгаЙиЮяжЪМфДцдкШчЯТЭМЫљЪОзЊЛЏЙиЯЕЃК
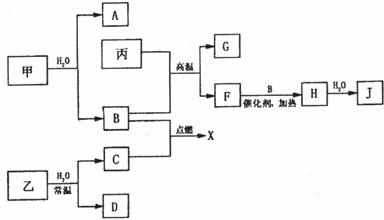
(1)ШєBгыCЗДгІЕФВњЮяXЮЊСНжжЮяжЪзщГЩЕФЛьКЯЮяЃЎИУЗДгІФмЗХГіДѓСПШШЃЌГЃгУгкКИНггыЧаИюН№ЪєЃЌИУЗДгІЕФЛЏбЇЗНГЬЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ШєBгыCЕФЗДгІВњЮяXЪЧДПОЛЮяЃЌЗДгІвВФмЗХГіДѓСПШШЃЌдђCЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(2)ЪЕбщЪвМьбщFЪБЃЌГЃгУЕФЪдМСЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌМьбщЙ§ГЬжаЙлВьЕНЕФЪЕбщЯжЯѓЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁ (3)JЕФЙЄвЕЩњВњЙ§ГЬжаЃЌFЁњHЕФЗДгІдкЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюЙЄвЕЩшБИУћГЦ)НјааЃКвбжЊБћгыBЗДгІЩњГЩ1molFЪБЗХГі426ЃЎ5KJЕФШШСПЃЌдђБћгыBЗДгІЕФШШЛЏбЇЗНГЬЪНЮЊ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃгЩБћжЦШЁlmol JЪБЃЌашвЊЯћКФЁЁЁЁЁЁ mol BЁЃ
[бЁзіВПЗж]
ЁЁЁЁ ЙВ8ИіЬтЃЌПМЩњДгжабЁдё2ИіЮяРэЬтЁЂ1ИіЛЏбЇЬтКЭ1ИіЩњЮяЬтзїД№ЁЃ
29ЃЎ(13Зж)
ЖЬжмЦкжїзхдЊЫиAЁЂBЁЂCЁЂDЕФдзгађЪ§вРДЮдіДѓЃЌЫќУЧЕФдзгКЫЭтЕчзгВуЪ§жЎКЭЮЊ7ЁЃ BЕФЛЏКЯЮяжжРрЗБЖрЃЌЪ§ФПХгДѓЁЃAгыDФмаЮГЩдзгИіЪ§БШЮЊlЃК1КЭ2ЃКlЕФЛЏКЯЮяЁЃ
(1)жЛгЩAЁЂBЁЂDзщГЩЕФЛЏКЯЮяжаЃЌЯрЖдЗжзгжЪСПзюаЁЕФЪЧЁЁЁЁЁЁЁЁЁЁ ЃЌаДГіИУЛЏКЯЮяЕФвЛжжгУЭОЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃШЫРрСљДѓгЊбјЫижаЃЌжЛгЩAЁЂBЁЂDШ§жждЊЫизщГЩЕФгаЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюЦфжавЛжжгЊбјЫиЕФУћГЦ)ЁЃ
ЁЁ (2)жЛгЩAЁЂCзщГЩЕФвЛжжГЃМћЦјЬЌЛЏКЯЮяЃЌЦфЕчзгЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁ
ЃЌЙЄвЕЩЯКЯГЩИУЦјЬхЕФЛЏбЇЗНГЬЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЃЭљЕШЬхЛ§ЕФIЁЂЂђСНИіУмБеШнЦїжаЗжБ№ГфШы1molAЕЅжЪКЭ1molCЕЅжЪЁЂ2molAЕЅжЪКЭ2molCЕЅжЪЁЃвЛЖЈЬѕМўЯТЃЌГфЗжЗДгІКѓЗжБ№ДяЕНЦНКт(СНШнЦїЮТЖШЯрЕШ)ЁЃе§ШЗБэЪОIЁЂЂђШнЦїжаAЕЅжЪЕФЮяжЪЕФСПЗжЪ§(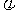 )ЫцЪБМф(t)БфЛЏЕФЪОвтЭМЪЧЁЁЁЁЁЁЁЁЁЁЁЁ
(ЬюБъКХ)ЁЃ
)ЫцЪБМф(t)БфЛЏЕФЪОвтЭМЪЧЁЁЁЁЁЁЁЁЁЁЁЁ
(ЬюБъКХ)ЁЃ
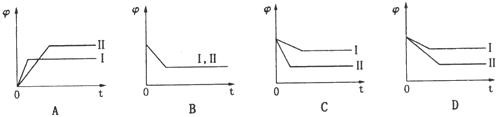
ЁЁ (3)жЛгЩAЁЂCЁЂDзщГЩЕФбЮЃЌЗЂЩњЫЎНтЗДгІЕФРызгЗНГЬЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(4)МзЁЂввСНжжЛЏКЯЮяЖМжЛгЩAЁЂBЁЂCЁЂDЫФжждЊЫизщГЩЃЌЫќУЧМШФмгыбЮЫсЗДгІгжФмгыЩеМюШмвКЗДгІЁЃЦфжаЃЌМзЮЊЮоЛњЫсЪНбЮЃЌМзгыЯЁЩеМюШмвКЗДгІЕФРызгЗНГЬЪНЪЧЁЁЁЁЁЁ ЁЁЁЁЁЁЃКввЮЊЬьШЛЕААзжЪЫЎНтЕФЯрЖдЗжзгжЪСПзюаЁЕФВњЮяЃЌЦфНсЙЙМђЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
28ЃЎ(15Зж)
ТСУОКЯН№вбГЩЮЊТжДЌжЦдьЁЂЛЏЙЄЩњВњЕШаавЕЕФживЊВФСЯЁЃбаОПадбЇЯАаЁзщЕФШ§ЮЛЭЌбЇЃЌЮЊВтЖЈФГКЌУО3%вЛ5%ЕФТСУОКЯН№(ВЛКЌЦфЫќдЊЫи)жаУОЕФжЪСПЗжЪ§ЃЌЩшМЦЯТСаШ§жжВЛЭЌЪЕбщЗНАИНјааЬНОПЁЃЬюаДЯТСаПеАзЁЃЁЁЁЁ
ЁЁ [ЬНОПвЛ]ЪЕбщЗНАИЃКТСУОКЯН№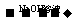 ВтЖЈЪЃгрЙЬЬхжЪСП
ВтЖЈЪЃгрЙЬЬхжЪСП
ЁЁЁЁ ЪЕбщжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁ ЪЕбщВНжшЃК
(1)ГЦШЁ5.4gТСУОКЯН№ЗлФЉбљЦЗЃЌЭЖШыVmL 2.0molЁЄLNaOHШмвКжаЃЌГфЗжЗДгІКѓNaOHШмвКЕФЬхЛ§VЁнЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(2)Й§ТЫЁЂЯДЕгЁЂИЩдяЁЂГЦСПЙЬЬхЁЃИУВНжшжаШєЮДЯДЕгЙЬЬхЃЌВтЕУУОЕФжЪСПЗжЪ§НЋ
ЁЁЁЁЁЁ (ЬюЁАЦЋИпЁБЛђЁАЦЋЕЭЁБ)ЁЃ
ЁЁЁЁЁЁ [ЬНОПЖў]
ЁЁЁЁЁЁ ЪЕбщЗНАИЃКТСУОКЯН№ ВтЖЈЩњГЩЦјЬхЕФЬхЛ§ЪЕбщзАжУЃК
ВтЖЈЩњГЩЦјЬхЕФЬхЛ§ЪЕбщзАжУЃК
ЁЁЁЁЁЁ ЮЪЬтЬжТлЃК
(1)ФГЭЌбЇЬсГіИУЪЕбщзАжУВЛЙЛЭъЩЦЃЌгІдкAЁЂBжЎМфЬэМгвЛИіИЩдяЁЂГ§ЫсЮэЕФзАжУЁЃФуЕФвтМћЪЧЃКЁЁЁЁЁЁЁЁЁЁ (ЬюЁАашвЊЁБЛђЁАВЛашвЊЁБ)ЁЃ
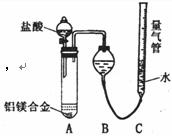
ЁЁ (2)ЮЊЪЙВтЖЈНсЙћОЁПЩФмОЋШЗЃЌЪЕбщжагІзЂвтЕФЮЪЬтЪЧ(аДГіСНЕу)ЃК
ЁЁЁЁЁЁЁЁ ЂйЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЂкЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁ [ЬНОПШ§]
ЪЕбщЗНАИЃКГЦСПx gТСУОКЯН№ЗлФЉЃЎЗХдкШчЯТЭМЫљЪОзАжУЕФЖшадЕчШШАхЩЯЃЌЭЈЕчЪЙЦфГфЗжзЦЩеЁЃ
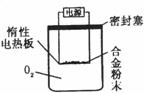
ЁЁЁЁЁЁ ЮЪЬтЬжТлЃК
ЁЁ (1)гћМЦЫуMgЕФжЪСПЗжЪ§ЃЌИУЪЕбщжаЛЙашВтЖЈЕФЪ§ОнЪЧЁЁЁЁ
ЁЁ (2)ШєгУПеЦјДњЬцO2НјааЪЕбщЃЌЖдВтЖЈНсЙћЪЧЗёгагАЯь?ЁЁЁЁЁЁ (ЬюЁАЪЧЁБЛђЁАЗёЁБ)ЁЃ
ЁЁЁЁЁЁ [ЪЕбщЭиеЙ]
ВЮееЬНОПвЛЁЂЬНОПЖўЪЕбщЗНАИЃЌЧыФуСэЩшМЦвЛИіЪЕбщЗНАИЃЌВтЖЈИУТСУОКЯН№жаУОЕФжЪСПЗжЪ§ЁЃ
ЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
15ЃЎдкЖўбѕЛЏЬМЕФЫЎШмвКжаДцдкзХШчЯТЦНКтЃК
ЁЁЁЁЁЁ CO2(g) CO2(aq)
CO2(aq)
ЁЁ ЁЁCO2(aq)+H2O H2CO3(aq)
H2CO3(aq)
ЁЁЁЁЁЁ H2CO3(aq) H+(aq)+HCO3-(aq)
H+(aq)+HCO3-(aq)
ЁЁ ЁЁHCO3-(aq) H+(aq)+CO32-(aq)
H+(aq)+CO32-(aq)
ЁЁЁЁЁЁ ЯТСагаЙиЫЕЗЈе§ШЗЕФЪЧ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎЫЎжаШмНтЕФЖўбѕЛЏЬМЕФХЈЖШЃЌЯФЬьЪББШЖЌЬьЪБИп
ЁЁЁЁЁЁ BЃЎШчЙћКЃЫЎТдГЪМюадЃЌКЃЫЎжаЖўбѕЛЏЬМЕФХЈЖШБШДПЫЎИп
ЁЁЁЁЁЁ CЃЎЦјбЙЩ§ИпЃЌЫЎжаc(HCO3-)діДѓ
ЁЁЁЁЁЁ DЃЎГЃЮТЯТЃЌЖўбѕЛЏЬМЕФЫЎШмвКжаЃЌгЩЫЎЕчРыГіЕФc(H+)гыc(OH-)ЕФГЫЛ§ЕШгк1ЁСl0-14
ЕкЂђОэ(Бизі120Зж+бЁзі32ЗжЃЌЙВ152Зж)
[БизіВПЗж]
14ЃЎРћгУЯТЭМЫљЪОзАжУжЦШЁFe(OH)2ЃЌЭЈЕчКѓШмвКжаВњЩњЕФАзЩЋГСЕэФмБЃГжНЯГЄЪБМфВЛБфЩЋЁЃЯТСаЫЕЗЈДэЮѓЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
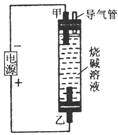
ЁЁЁЁЁЁ AЃЎЩеМюШмвКзЂШыШнЦїЧАЃЌашдЄЯШжѓЗа
ЁЁЁЁЁЁ BЃЎМзЕчМЋЩЯгаЧтЦјУАГі
ЁЁ ЁЁЁЁ CЃЎжЛФмгУЬњзїМзЕчМЋКЭввЕчМЋ
ЁЁЁЁЁЁ DЃЎПЩгУЪГбЮЫЎДњЬцЩеМюШмвК
13ЃЎвЛЖЈЬѕМўЯТЃЌАБЦјгыЗњЦјЗЂЩњЗДгІЃК4NH3+3F2=NF3+3NH4FЃЌЦфжаNF3ЗжзгЙЙаЭгыNH3ЯрЫЦЁЃЯТСагаЙиЫЕЗЈДэЮѓЕФЪЧЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁ ЁЁЁЁ AЃЎNF3ЪЧМЋадЗжзг
ЁЁЁЁЁЁ BЃЎNF3МШЪЧбѕЛЏВњЮяЃЌгжЪЧЛЙдВњЮя
ЁЁ ЁЁЁЁ CЃЎNH4FжаМШКЌгаРызгМќгжКЌгаЙВМлМќ
ЁЁ ЁЁЁЁ DЃЎЩЯЪіЗДгІжаЃЌЗДгІЮяКЭЩњГЩЮяОљЪєгкЗжзгОЇЬх
12ЃЎЮоЩЋПзШИЪЏТЬ(НсЙЙМђЪНШчЯТЭМЫљЪО)дјБЛгУзїЫЎВњбјжГвЕЕФЩБГцМС(гувЉ)ЁЃвђЮЊОпгаЧБдкжТАЉадЃЌвбБЛНћжЙгУзїгувЉЁЃЯТСаЙигкЮоЩЋПзШИЪЏТЬЕФа№ЪіжаЃЌе§ШЗЕФЪЧ(ЁЁ ЁЁ)
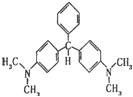
AЃЎЗжзгжаЧтдзгЪ§ЮЊЦцЪ§
ЁЁЁЁЁЁ BЃЎЗжзгжаЫљгаЕФЬМдзгПЩФмдкЭЌвЛЦНУцЩЯ
ЁЁЁЁЁЁ CЃЎгыБНАЗ(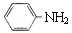 )ЛЅЮЊЭЌЯЕЮя
)ЛЅЮЊЭЌЯЕЮя
ЁЁЁЁЁЁ DЃЎдквЛЖЈЬѕМўЯТЃЌ1 molЮоЩЋПзШИЪЏТЬПЩвдКЭ9molЧтЦјЗЂЩњМгГЩЗДгІ
11ЃЎЭЈЙ§жУЛЛЗДгІВЛПЩФмЩњГЩЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎFe3O4ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎF2ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎAl2O3ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎC
10ЃЎФГc(H+)=1ЁС10-2molЁЄL-1ЕФШмвКжаКЌгаДѓСПNO3-ЁЂSO42-ЃЌИУШмвКжаЛЙПЩФмДѓСПДцдкЕФРызгЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎNH4+ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎI-ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎBa2+ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎC6H5O-
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com