
11.常温下,有甲、乙两份体积均为1L、浓度均为0.1mol·L-1的氨水,其pH为11.①甲用蒸馏水稀释100倍后,溶液的pH将为a;②乙与等体积、浓度为0.2mol·L-1的HCl混合,在混合溶液中: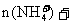 n(H-)-n(OH-)=bmol则a、b分别为 ( )
n(H-)-n(OH-)=bmol则a、b分别为 ( )
A.9-11之间 0.1 B.9-11之间 0.2
C.12-13之间 0.2 D.13 0.1
10.下列叙述中不正确的是 ( )
A.固体氯化钠不能导电,但氯化钠是电解质
B.纯水的pH随温度的升高而减小
C.在醋酸钠溶液中假如少量氢氧化钠,溶液中c(OH-)增大
D.在纯水中加入少量硫酸和硫酸铵,均可抑制水的电离
9.往4.5mL的某硝酸银溶液中加入一定量pH=1的盐酸,恰好将溶液中的Ag完全沉淀,加水稀释,得到pH=2的溶液50.0mL,则该硝酸银溶液的浓度为 ( )
A.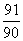 mol·L-1 B.
mol·L-1 B.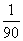 mol·L-1 C.
mol·L-1 C.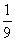 mol·L-1 D.
mol·L-1 D.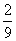 mol·L-1
mol·L-1
8.下列关于粒子结构的描述中不正确的是 ( )
A.H2S和NH3均是电子总数为8的极性分子
B.HS-和HCl均是含有一个极性键的18电子粒子
C.CH2Cl2和CCl4均是四面体构型的非极性分子
D.1molD216O中含中子、质子、电子各10NA(NA表示阿伏伽德罗常数)
7.设NA为阿伏伽德罗常数,下列说法正确的是 ( )
A.标准状况下,含1molHCl和氢氟酸的混合物的体积约为22.4L
B.电解精炼铜时,当转移1mol电子时,阳极材料质量减轻了32g
C.1.72生石膏(CaSO4·2H2O)转化为熟石膏(2CaSO4·2H2O)失去的结晶水数目为0.015NA
D.9g重水含有的电子数为5NA
6.下列分散系中,分散质微粒直径最大的是 ( )
A.雾 B.石灰乳 C.氢氧化铁胶体 D.淀粉溶液
29.(14分)已知一个碳原子上连有两个羟基时,易发生下列转化:
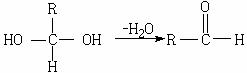 请根据下图回答。
请根据下图回答。
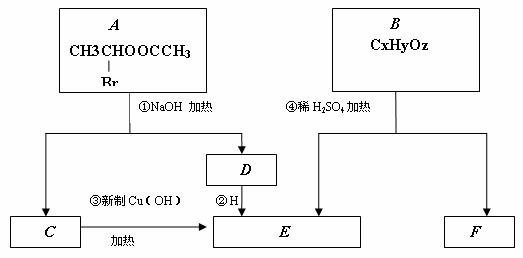
(1)E中含有官能团的名称是 ;③的反应类型是 ,C跟新制的氢氧化铜反应的化学方程式为 ;
(2)已知B的相对分子质量为162,其燃烧产物中n(CO2):n(H2O)=2:1则B的分子式为 ,F的分子式为 。
(3)在电脑芯片生产领域,高分子光阻剂是光刻蚀0.11μm线宽芯片的关键技术。F是这种高分子光阻剂生产中的主要原料。F具有如下特点:①能跟FeCl3溶液发生显色反应:②能发生加聚反应;③芳环上的一氯代物只有两种。F在一定条件下发生加聚反应的化学方程式为 。
(4)化合物G是F的同分异构体,它属于芳香族化合物,能发生银镜反应。G可能有 种结构,写出其中任一种同分异构体的结构简式 。
28.(12分)用下图装置进行SO2转化为SO3的转化率测定实验:
2SO2+O2 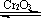 2SO3 △H=-196.6kJ/mol
2SO3 △H=-196.6kJ/mol
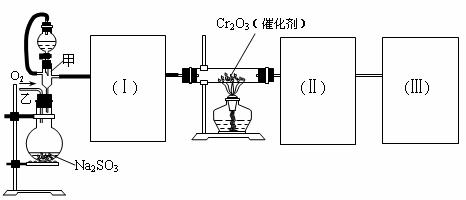
(1)要顺利进行实验,上图Ⅰ、Ⅱ、Ⅲ处各应连接1个合适的装置,请从下列A~E中选择适宜的装置,将其序号填入空格内。Ⅰ 、Ⅱ 、Ⅲ 。
(2)实验前,必须进行的操作是(填操作名称,不必写具体过程)
(3)实验时,浓硫酸能顺利滴入烧瓶中,甲装置所起作用的原理是:
(4)从乙处均匀通入O2,为使SO2有较高的转化率,实验时滴入浓硫酸与加热催化剂的先 后顺序是 。
(5)实验中当Cr2O3表面红热时,应将酒精灯移开一会儿再加热,以防温度过高,这样做的原因是 Cr2O3处的反应管时,SO2的转化率会 (填升高、降低或不变)
(6)实验时若用25.2g的Na2SO3,加入的浓硫酸是足量的,反应结束时继续通入O2一段时间,称得Ⅱ处装置的质量增加11.3g,则本实验中SO2的转化率为 。(保留3位有效数字)
27.已知C、D、E、H为气体,反应①是工业生产中的重要反应,反应④⑥⑧是实验室重要的物质检验反应,这些物质有如图所示的转化关系(生成物中的水均已略出)。
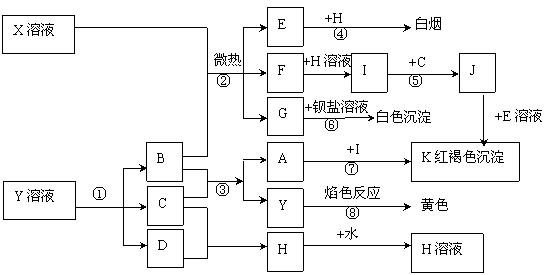
 试回答:
试回答:
(1)写出化学式:K: H:
(2)反应⑦中A溶液显示的性质是 (填序号:A.氧化性;B.还原性;C酸性;D.碱性)
(3)若X是一种复盐(不考虑结晶水),X的化学式为: 。
(4)写出下列反应的离子方程式:
反应② ;
反应③ ;
反应⑤ 。
26.(14分)(I)某同学拟用下图装置分别制取H2和NO。而实验室只有水、浓硫酸、浓硝酸、铜片。①制取H2时,还缺少的固体试剂是 ,(填名称)反应的离子方程式: ;
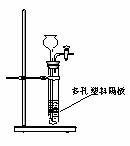
②制取NO时,请你从上述试剂中为他选择比较合理的试剂是 ;反应产生的气体需要用 法收集。
(II)有一份由两种物质混合而成的白色混合物,分别取适量该混合物置于三支试管中进行实验。
①加热第一支试管中的白色混合物,试管口有水滴凝结
②在第二支试管中逐滴加入4mol·L-1的NaOH溶液至过量,
同时不断振荡试管,有气泡产生,反应结束后试管中还有白色不溶物
③在第三支试管中逐滴加入4mol·L-1盐酸,同时不断振荡试管,有无色无味的气体产生,反应结束后得到无色透明溶液
(1)符合以上实验现象的是 混合物(填选项);
A.NaHCO3、AgNO3 B.BaCl2、MgCO3
C.NH4HSO3、MgCl2·6H2O D.NH4Cl、Ca(HCO3)2
(2)该混合物中的某一成分水溶液的pH<7,该物质是: (填化学式);
(3)该混合物在实验②中产生白色不溶物的离子方程式: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com