
34.(9分)(1)现将乙醇、O2、铂电极和KOH溶液构成燃料电池以提高燃料的利用率。电池的总反应类似于CH4在O2中燃烧,电池放电过程中,溶液pH不断减小,则负极反应的离子方程:________________。
(2)含氮废水进入水体后对环境造成的污染越来越严重。对含氮废水进行有效的检测和合理的处理是人们研究和关心的重要问题。经环境专家测定:
①在水溶液中,在微生物作用下NH3转化为NO3-,溶液的pH变小,有关离子方程式_________________。
②用金属铝可将水体中的NO3- 还原为N2,从而消除污染。其反应的离子方程式是:
10Al+6NO3-+18H2O=3N2↑+10Al(OH)3+6OH-。有人认为金属镁比铝能更快消除氮的污染,其反应原理和金属铝相同。则镁和含NO3-的废水反应的离子方程式____________________。
33.(12分)下图为中学化学常见的几种物质的转化关系。已知各物质所含元素均为短周期元素,且甲、乙为单质,A、B、C、D为化合物,其中C为白色难溶于水的固体,D在常温下为气体。试回答下列问题:
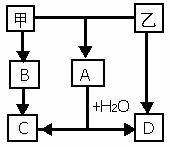
(1)下面关于相关的物质的说法中不正确的是:
a.甲可能为金属,也可能为非金属
b.乙一定为非金属单质,D一定为非金属氢化物
c.A可能为离子化合物,也可能为共价化合物
d.B不可能为氧化物
e.C可能为酸,也可能为碱
(2)若C既能溶于酸,又能溶于碱,且D是18电子分子,则A的化学式为: ___________
写出一种实现甲→B→C两步变化的离子方程式: __________________________。
(3)若C不溶于碱,但可溶于酸,且D为碱性气体,A溶于足量盐酸可生成两种盐,这两种盐的化学式为:_______________、_____________
(4)若C不溶于强酸,但可溶于强碱,且甲的晶体是良好的半导体材料,乙为常见有色气体,且A为非极性分子,则A与水反应的化学方程式为: ____________________。
32.(9分)化学与工农业生产、日常生活紧密相关。
Ⅰ.侯氏制碱法所得纯碱样品中往往只含有少许NaCl杂质,现欲测定其中Na2CO3的质量分数,分别设计了如下实验方案。
A:沉淀分析法
把一定量的样品溶解后加入过量CaCl2,将所得沉淀过滤、洗涤、烘干、称量。
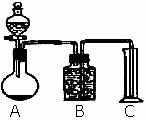
B:气体分析法(用上图装置)
把一定量的混合物与足量硫酸反应后,用如图装置测定产生的CO2气体的体积。
C:中和滴定法
用已知浓度的硫酸或盐酸,滴定一定量的未知浓度的Na2CO3溶液(用甲基橙或酚酞做指示剂),
(1)上述方法中,综合考虑,你认为较好的是:____________。
(2)对上述方法的叙述,你认为合理的是:________________。
a.A测定的结果较准确,但操作复杂
b.B操作比较简单,但测定结果不太准确
c.C操作比较简单,测定的结果较准确
d.A、B、C测定的结果都不准确
Ⅱ.某研究性学习小组查阅资料得知,漂白粉溶液与硫酸溶液反应可制取氯气,他们设计了如下图制取氯气并验证其性质的实验装置。请回答下列问题:
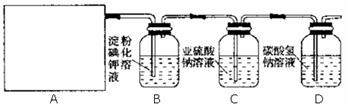
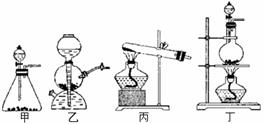
(1)该实验中A部分的装置是 (填写装置的序号)A中发生的化学反应方程式__________
(2)检验C中的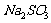 已被氧化的试剂(不必简述实验步骤):_______(填化学式)
已被氧化的试剂(不必简述实验步骤):_______(填化学式)
31.(10分)A、B、C、D、E、F六种元素,原子序数依次增大。A可形成A-或A+,B在自然界中形成的化合物种类最多,C在自然界中形成的氧化物种类最多,D在地壳中含量最高,E-不易被任何氧化剂氧化,F在短周期中原子半径最大。六种元素的原子彼此能形成多种微粒,试用这些微粒填空。
(1)写出常见的两核18e-微粒的化学式:阴离子:_______分子:_________
(2)写出两种常见的能促进水电离的五原子离子的化学式:___________、_________
(3)写出两种常见的10e-的微粒间反应的离子方程式:____________________________
30.在托盘天平的左右的两托盘中各放置一只烧杯,调节天平使之平衡,向烧杯中分别注入足量且等质量、等浓度的稀硫酸,然后向两只烧杯中分别加入等质量或等物质的量的A和B,反应完成后,天平仍保持平衡,则A、B一定不可能是:
A.Na Mg B.KHCO3 CaCO3 C.MgO MgCO3 D.Na2CO3 NaHCO3
第Ⅱ卷(非选择题,共40分)
29.常温下跟镁粉、溴水、氯化铁溶液、硝酸都能发生氧化还原反应的是:
A.Na2S溶液 B.K2SO4溶液 C.(NH4)2SO3饱和溶液 D.NaOH溶液
28.某氧化还原反应中,反应物和生成物共五种:NO、SO2、HNO3、H2SO4、H2O,则对该氧化还原反应的叙述正确的是:
A.反应的离子方程式:3SO2+2NO3-+2H2O =2NO↑+4H++3SO42-
B.NO是还原剂,SO2是还原产物
C.SO2是还原剂,NO是还原产物
D.当转移1mole-时,有1molH+生成
27.下列各组离子,在给定条件下一定能够大量共存的是:
A.在碱性溶液中:I-、Cl-、NO3-、Na+
B.使紫色石蕊试液显红色的溶液中:K+、F-、NO3-、Br-
C.含有大量Fe3+的溶液中:Na+、Mg2+、CO32-、SCN-
D.水电离出的c(H+)=1×10-13mol·L–1的溶液中:Na+、Ba2+、NO3-、OH-
26.下列离子方程式书写正确的是:
A.NaHCO3溶液水解:HCO3-+H2O CO32-+H3O+
CO32-+H3O+
B.向澄清石灰水中通入过量的CO2:Ca+2OH-+CO2=CaCO3↓+2H2O
C.向Na2CO3溶液中滴入少量明矾溶液:Al3++3CO32-+3H2O=Al(OH)3↓+3HCO3-
D.向NaClO溶液中通入少量的SO2:ClO-+SO2+H2O=2H++Cl-+SO42-
25.甲、乙是由短周期元素组成的常见物质或微粒,在中学化学中有许多物质或微粒能满足下列相互转化关系: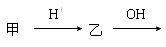 下列说法正确的是:
下列说法正确的是:
A.若乙为无色无味气体,则甲一定是CO32-
B.若甲是具有刺激性气味的气体,则甲、乙具有相同的电子数
C.若甲、乙均为离子,甲、乙两种离子在同一溶液中一定不能大量共存
D.甲有可能是AlO2- 也有可能是Al(OH)3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com