
8£®ÔÚÓĞ´ß»¯¼Á´æÔÚµÄÌõ¼şÏ£¬½«2Ìå»ıSO2ºÍ1Ìå»ıµÄO2»ìºÏ×°ÈëÃܱÕÈİÆ÷Öв¢¼ÓÈÈÒ»¶Îʱ¼äºó£¬½«»ìºÏÆøÌåͨÈëBaCl2ÈÜÒºÖĞ£¬²úÉúµÄ³Áµí¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡¡¡¡¡ A£®²»¿ÉÄÜÊÇBaSO4¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ B£®Ò»¶¨ÊÇBaSO3
¡¡¡¡¡¡ C£®Ò»¶¨ÊÇBaSO4¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ D£®Ò»¶¨ÊÇBaSO3ºÍBaSO4
7£®ÔªËØAµÄÑôÀë×ÓÓëÔªËØBµÄÒõÀë×Ó¾ßÓĞÏàͬµÄµç×Ó²ã½á¹¹¡£ÒÔϹØÓÚA¡¢BÔªËصıȽÏÖĞ£¬²»ÕıÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡¡¡¡¡ A£®Ô×Ӱ뾶£ºA<B¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ B£®Ô×ÓĞòÊı£ºA>B
¡¡¡¡¡¡ C£®Ô×Ó×îÍâ²ãµç×ÓÊı£ºB>A¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ D£®ÔªËØËùÔÚµÄÖÜÆÚÊı£ºA>B
6£®¡°ĞÅÏ¢¡±¡¢¡°²ÄÁÏ¡±ºÍ¡°ÄÜÔ´¡±±»³ÆΪĞ¿Ƽ¼¸ïÃüµÄÈı´óÖ§Öù¡£ÏÂÁĞÓйØ×ÊѶ´íÎóµÄÊÇ
A£®ÔÚ¼´½«µ½À´µÄĞÂÄÜԴʱ´ú£¬ºËÄÜ¡¢Ì«ÑôÄÜ¡¢ÇâÄܽ«³ÉΪÖ÷ÒªÄÜÔ´
B£®ºÏ³É¸ß·Ö×Ó²ÄÁϵĹ㷺ӦÓÃÊÇÓĞ°ÙÀû¶øÎŞÒ»º¦
C£®2005Äê10ÔÂ12ÈÕ·¢Éä³É¹¦µÄ¡°ÉñÖÛÁùºÅ¡±ÔØÈË·É´¬Ê¹ÓÃÁË´óÁ¿µÄ¸´ºÏ²ÄÁÏ
D£®Ä¿Ç°ÖĞÃÀÈյȹúÕÆÎÕµÄÌÕ´É·¢¶¯»ú¼¼Êõ£¬´ó´óÌá¸ßÁË·¢¶¯»úµÄÄÜÁ¿×ª»¯Ğ§ÂÊ
5£®ÏÂÁĞ˵·¨ÖĞ´íÎóµÄÊÇ¡¡
A£®½«SO2ºÍCl2·Ö±ğͨÈëʯÈïÊÔÒººó£¬Ê¯ÈïÊÔÒº¶¼ÊÇÏȱäºìºóÍÊÉ«
B£®ÏòäåË®ºÍµâË®ÖĞ·Ö±ğ¼ÓÈëÉÙÁ¿CCl4ºó£¬Ï²ãµÄÑÕÉ«¶¼±ÈÉϲãÉî
C£®ÍË¿ºÍÌúË¿·Ö±ğÔÚÂÈÆøÖĞȼÉÕʱ£¬¶¼ÄܲúÉú×Ø»ÆÉ«µÄÑÌ
D£®ÁòËáºÍÏõËá·Ö±ğÈܽâÌúĞâʱ£¬¶¼»áÓĞ»ÆÉ«ÈÜÒº³öÏÖ
4£®½º×´ÒºÇâ(Ö÷Òª³É·ÖÊÇH2ºÍCH4)ÓĞÍûÓÃÓÚδÀ´µÄÔËÔØ»ğ¼ıºÍ¿Õ¼äÔËÊäϵͳ¡£ÊµÑé²âµÃ£¬101 kPaʱ£¬1 mol H2ÍêȫȼÉÕÉú³ÉҺ̬ˮ£¬·Å³ö285.8 kJµÄÈÈÁ¿£»1 mol CH4ÍêȫȼÉÕÉú³ÉҺ̬ˮºÍCO2£¬·Å³ö890.3 kJµÄÈÈÁ¿¡£ÏÂÁĞÈÈ»¯Ñ§·½³ÌʽÊéĞ´ÕıÈ·µÄÊÇ
A£®CH4(g)+2O2(g)===CO2(g)+2H2O(l)£»¦¤H=+890.3 kJ¡¤mol-1
¡¡¡¡ B£®CH4(g)+2O2(g)===CO2(g)+2H2O(l)£»¦¤H=-890.3 kJ¡¤mol-1
¡¡¡¡ C£®CH4(g)+2O2(g)===CO2(g)+2H2O(g)£»¦¤H=-890.3 kJ
¡¡¡¡ D£®2H2(g)+O2(g)=== 2H2O(l)£»¦¤H=-285.8 kJ
3£®2007Äêŵ±´¶û»¯Ñ§½±ÊÚÓèµÂ¹ú»¯Ñ§¼Ò¸ñ¹şµÂ•°£ÌضûÊÇÒòΪËûÔÚ±íÃ滯ѧËù×÷µÄ¿ª´´ĞÔÑо¿£¬ËûµÄ·½·¨²»½ö±»ÓÃÓÚѧÊõÑо¿¶øÇÒ±»ÓÃÓÚ»¯Ñ§¹¤ÒµÑĞ·¢¡£ÏÂÃæÑ¡ÏîÓëÎïÖʵıíÃæÌØĞÔÎŞ¹ØµÄÊÇ
A£®ºÏ³É°±ÓÃÌú·Û×ö´ß»¯¼Á¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
B£®ÓÃÃ÷·¯À´¾»Ë®
C£®Óû¹ÔÌú·ÛºÍÊ¯ÃŞÈŞ»ìºÏÎïÓëË®ÕôÆøÖƵÃFe3O4ºÍH2
D£®ÅäÖÆFeCl3 ÈÜҺʱ½«FeCl3¹ÌÌåÈÜÓÚŨÑÎËáÖĞÔÙ¼ÓˮϡÊÍ
2£®ÏÂÁĞÑ¡ÏîÓ뽺ÌåÖªÊ¶ÎŞ¹ØµÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡¡¡¡¡ A£®ÔÚ¶¹½¬Àï¼ÓÈëÑα×ö¶¹¸¯
¡¡¡¡¡¡ B£®Ë®Äà¡¢Ò±½ğ³§³£Óøßѹµç³ıÈ¥¹¤³§Ñ̳¾£¬ÒÔ¼õÉÙ¶Ô¿ÕÆøÎÛȾ
¡¡¡¡¡¡ C£®Ò»ÊøƽĞйâÏßÕÕÉä°µÏäÖеĵ°°×ÖÊÈÜҺʱ£¬´Ó²àÃæ¿ÉÒÔ¿´µ½¹âÁÁµÄͨ·
¡¡¡¡¡¡ D£®ÂÈ»¯ÂÁÈÜÒºÖмÓÈëĞ¡ËÕ´òÈÜÒº»á²úÉú°×É«³ÁµíºÍÆøÌå
1£®¸ÖÌúÔÚ³±Êª¿ÕÆøÖĞ·¢Éúµç»¯Ñ§¸¯Ê´Ê±£¬Õı¼«·¢ÉúµÄÖ÷Òª·´Ó¦ÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡¡¡¡¡ A£®Fe£2e-=Fe2+¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ B£®2H2O+O2+4e-=4OH-
¡¡¡¡¡¡ C£®4OH--=2H2¡¡ O+O2+4e¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ D£®2H++2e-=H2
27£® Ğ¿ÊÇÒ»ÖÖÖØÒªµÄ½ğÊô£¬Ğ¿¼°Æ仯ºÏÎïÓĞ׏㷺µÄÓ¦Óá£
(1)ÆÏÌÑÌÇËáĞ¿[CH2OH(CHOH)4COO]2ZnÊÇÄ¿Ç°Êг¡ÉÏÁ÷ĞеIJ¹Ğ¿¼Á¡£Ğ´³öZn2+»ù̬µç×ÓÅŲ¼Ê½¡¡¡¡¡¡¡¡¡¡¡¡ £»ÆÏÌÑÌÇ[CH2OH(CHOH)4CHO]·Ö×ÓÖĞ̼Ô×ÓÔÓ»¯·½Ê½ÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
¡¡(2)Zn2+Ò²ÄÜÓëNH3ĞγÉÅäÀë×Ó[Zn(NH3)4]2+¡£ÅäλÌåNH3·Ö×ӿռ乹ĞÍΪ¡¡¡¡¡¡¡¡¡¡ £»ÔÚ[Zn(NH3)4]2+ÖĞ£¬Zn2+λÓÚÕıËÄÃæÌåÖĞĞÄ£¬NλÓÚÕıËÄÃæÌåµÄ¶¥µã£¬ÊÔÔÚÏÂͼÖбíʾ[Zn(NH3)4]2+ÖĞZn2+ÓëNÖ®¼äµÄ»¯Ñ§¼ü¡£
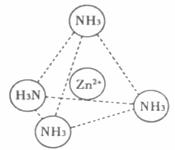
(3)ÏÂͼ±íʾпÓëijÖÖÔªËØXĞγɵĻ¯ºÏÎᄃ°û£¬ÆäÖĞZnºÍXͨ¹ı¹²¼Û¼ü½áºÏ£¬¸Ã»¯ºÏÎïµÄ»¯Ñ§Ê½Îª¡¡¡¡¡¡¡¡¡¡¡¡¡¡ £»
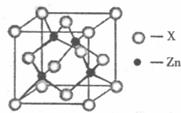
¸Ã»¯ºÏÎïµÄ¾§ÌåÈÛµã±È¸É±ù¸ßµÃ¶à£¬ÔÒòÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
26£®·Ò±ØµÃÊÇÒ»ÖÖ½âÈÈÕòÍ´Ò©ÎÆäÓĞЧ³É·ÖÊDz¼Âå·Ò(Ibuprofen)¡£ÏÂÁĞÊÇij¹«Ë¾Ğ·¢Ã÷µÄ²¼Âå·Ò(Ibuprofen)ÂÌÉ«ºÏ³É·½·¨Á÷³Ìͼ(·´Ó¦Ìõ¼şÊ¡ÂÔ)¡£
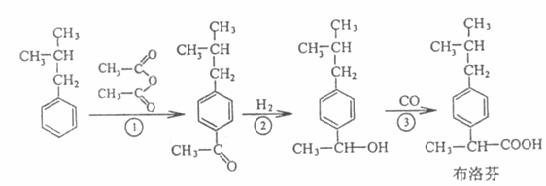
ÊԻشğÏÂÁĞÎÊÌ⣺
(1)²¼Âå·Ò·Ö×ÓÖĞÓĞ¡¡¡¡¡¡¡¡¡¡ ¸öÊÖĞÔ̼Ô×Ó¡£
(2)·´Ó¦¢ÙÊôÓÚÈ¡´ú·´Ó¦£¬ÊÔĞ´³ö·´Ó¦¢ÙµÄ»¯Ñ§·½³Ìʽ£º¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(3)·´Ó¦¢ÚµÄ·´Ó¦ÀàĞÍÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ·´Ó¦¡£
(4)Óë²¼Âå·Ò»¥ÎªÍ¬·ÖÒì¹¹ÌåµÄ·¼Ïã×廯ºÏÎïÖĞÓĞÒ»ÀàÊôÓÚõ¥£¬Æä½á¹¹¿É±íʾΪ£º
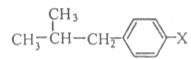 ÔòXµÄ½á¹¹ÓĞ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡ÖÖ(ÌîÊı×Ö)¡£
ÔòXµÄ½á¹¹ÓĞ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡ÖÖ(ÌîÊı×Ö)¡£
(5)ÒÑÖªReppe·´Ó¦£º
ijѧÉúÌáÒéÓÃRePPe·´Ó¦Ò»²½ºÏ³É²¼Âå·Ò£¬²¢Ê¹Ô×ÓÀûÓÃÂÊΪ100%£¬Ğ´³öÓÃÒ»ÖÖÓĞ»úÎï(ÆäËüÎŞ»úÊÔ¼ÁÈÎÑ¡)Ò»²½ºÏ³É²¼Âå·ÒµÄ»¯Ñ§·½³Ìʽ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
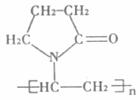
(6)¾ÛÒÒÏ©ßÁ¿©ÍéͪÊǷұصÃÖеĸ¨ÁÏ£¬Æä½á¹¹¼òʽÈçÏÂͼ¡£ÊÔĞ´³ö¾ÛÒÒÏ©Åø¿©ÍéͪÔÚÒ»¶¨Ìõ¼şÏÂË®½â²úÎïµÄ½á¹¹¼òʽ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
¹ú¼ÊѧУÓÅÑ¡ - Á·Ï°²áÁбí - ÊÔÌâÁбí
ºş±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĞÅÏ¢¾Ù±¨Æ½Ì¨ | ÍøÉÏÓк¦ĞÅÏ¢¾Ù±¨×¨Çø | µçĞÅթƾٱ¨×¨Çø | ÉæÀúÊ·ĞéÎŞÖ÷ÒåÓк¦ĞÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĞÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com