
4.设NA表示阿伏加德罗常数,下列叙述中正确的是 ( )
A.1.8g重水(D2O)中含NA个中子
B.1.8g的NH+4离子中含有的电子数为NA
C.1molC8H18分子中共价键总数为23NA
D.标准状况下的22.4L辛烷完全燃烧,生成二氧化碳分子数为8NA
3.“可燃冰”是天然气与水在低温、高压条件下形成的,外貌极像冰雪或固体酒精,点火即可燃烧的一种固体物质,又被称为“气冰”、“固体瓦斯”。正式名称为天然气水合物(Natural Gas Hydrate,简称Gas Hydrate),又称笼形包合物(Clathrate)。被科学家们誉为“未来最理想的洁净能源”。下列说法错误的是 ( )
A.甲烷是最小的有机分子,是含氢量最高的有机物
B.甲烷是饱和链烃,化学性质稳定,在一定条件下可以发生取代反应
C.一个甲烷分子中含有4个C-H极性键,甲烷是由极性键形成的极性分子
D.甲烷的温室效应约是二氧化碳的20倍
2.工业制硫酸时,接触室中装有热交换器,下列叙述与热交换器作用有关的是 ( )
A.防止催化剂中毒
B.降低温度,减小反应的速度
C.充分利用能量,降低生产成本,提高综合经济效益
D.有利于平衡向正反应方向移动,提高原料利用率
1.下列电子式中书写正确的是 ( )
A.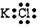 B.
B.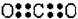 C.
C.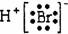 D.
D.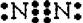
29.(16分)甲、乙、丙、丁、戊,五种短周期元素,它们的原子序数一次增大,其中甲与丁及丙与戊分别是同主族元素,乙与丙为相邻元素原子序数差为1;丙、戊两元素原子核内质子数之和是甲、丁两元素原子核内质子数之和的2倍。丙单质气体为通常能助燃的气体。据此回答下列问题
(1)甲、丙两元素可形成化合物A,其分子由四原子核构成,此分子的电子式为 , 已知A溶液显很弱酸性,写出A在水中的电离方程式 。
(2)写出由甲、丙、戊三种元素形成的六原子核化合物B的水溶液和A的水溶液反应的化学方程式 。
(3)由甲、乙、丙三种元素组成的常见无机化合物,写出一种由三种元素形成的常见无机酸(填化学式) ,其溶于水后对水的电离起 (填“抑制”、“促进”、“不影响”)作用。
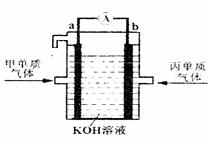
(4)用甲的单质和丙的单质支撑的燃料电池由于发电效率高而备受关注,其装置如下图所示。两个电极均由多孔惰性金属电极制成,用KOH溶液作电解质,通入气体并在电极表面放电。则a是 极,该燃料电池的总反应的化学方程式为: 。
28.(14分)由于Ca(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀。用如下图所示电解实验可制得的白色纯净的Fe(OH)2沉淀。两电极的材料分别为石墨和铁。
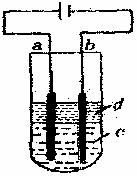
(1)a电极材料应为 ,电极反应式为 。
(2)电解液c可以是(填编号) 。
A.纯水 B.NaCl溶液 C.NaOH溶液 D.CuCl2溶液
(3)d为苯,其作用为 ,在加入苯之前对c溶液作何简单处理 (填编号)
①加入冰块降温处理 ②将c溶液加热煮沸处理 ③将c溶液无限稀释
(4)为了在较短时间内看到白色沉淀,可采取的措施 (填编号)
A.改用稀硫酸作电解液 B.适当增大电源的电流
C.适当减少两电极间距离 D.适当降低电解液的温度
(5)若c为Na2SO4溶液,当电解一段时间看到白色Fe(OH)2沉淀后,再反接电源电解,除了电极上看到气泡外,沉淀物的另一明显现象为 。
27.(14分)某实验室有:
仪器或用品:a.铁架台(含铁圈、各式铁夹)b.锥形瓶 c.酸式滴定管和碱式滴定管
d.烧杯(若干)e.玻璃棒 f.胶头滴管 g.天平(含砝码) h.滤纸
i.量筒 j.过滤漏斗 k.移液管
试剂: A.NaOH固体 B.标准NaOH溶液 C.未知浓度盐酸 D.蒸馏水
E.碳酸钠溶液 F.氯化镁溶液
试填空:
(1)进行过滤操作时,应选用的上述仪器或用品是 (选填序号)
(2)配置100mL2.0mol/L的氢氧化钠溶液时,还缺少的玻璃仪器是 。
(3)测定未知浓度盐酸的浓度时,还缺少的试剂是 。
(4)进行和滴定时,事先不能用待测的溶液润洗的玻璃仪器是 (选填序号)
(5)除去Mg(OH)2中混有的商量Ca(OH)2,可以用的试剂是: (选填序号),几个基本操作是 。
26.(16分)如下图,甲、乙、丙分别表示在不同条件下可逆反应:A(g)+B(g) xC(g)的生成物C在反应混合物中的百分含量(C%)和反应时间(t)的关系。
xC(g)的生成物C在反应混合物中的百分含量(C%)和反应时间(t)的关系。
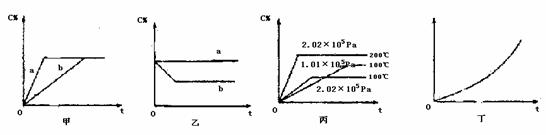
(1)若甲图中两条曲线分别代表有催化剂和无催化剂的情况,则 曲线表示无催化剂时的情况,速率:a b(填:大于、小于或等于)
(2)若乙图表示反映达到平衡后,分别在恒温恒压条件下和恒温恒容条件下向平衡混合气体中充入He气后的情况,则 曲线表示恒温恒容的情况,此时该恒温恒容中C% (填:变大、表小或不变)
(3)根据丙图可以判断该可逆反应的正反应是 热反映(填:发热、吸热),计量数值x的值 ;
(4)丁图表示在某固定容器的密闭容器中,上述可逆反应达到平衡后,某物理量随着温度(T)的变化情况,根据你的理解,丁图的纵坐标可以是 ,[填:①C% ②A的转化率 ③B的转化率 ④压强 ⑤c(A) ⑥c(B)];升温平衡移动的方向为 。(填:左移或右移)
13.已知反应:2SO2(g)+O2(g) 2SO3(g)△H=-196.6kJ/mol。测得体系中投入4mol
SO2和足量O2时,放热为314.5kJ,则SO2的转化率为 ( )
2SO3(g)△H=-196.6kJ/mol。测得体系中投入4mol
SO2和足量O2时,放热为314.5kJ,则SO2的转化率为 ( )
A.40% B.50% C.80% D.100%
第Ⅱ卷(非选择题)
12.已知外电路中,电子由铜流向a极。有关下图所示的装置分析合理的一项是 ( )
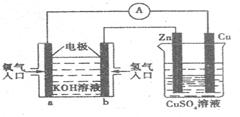
A.该装之中Cu极为正极
B.当铜片的质量变化为12.8g时,a极上消耗的O2在标准状况下的体积为2.24L
C.b极的电极反应式:H2-2e-=2H+
D.一段时间后锌片质量减少
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com