
14.下列叙述正确的是:
A.向某溶液中加入Ba(NO3)2溶液,有白色沉淀生成,再加稀盐酸,沉淀不溶解,说明有SO42-存在。
B.将SO2气体通入酸性 KMnO4溶液,KMnO4溶液褪色,说明SO2有漂白性。
C.量取20.00 mL lmol·L一1NaOH溶液:选用25mL碱式滴定管
D.向某溶液中加入盐酸,有气体产生,将产生的气体通入澄清石灰水,石灰水变浑浊,说明有CO32-存在。
13.下列离子方程式正确的是
A.向100 mL3 mol·L的FeBr2溶液中通入标准状况下4.48L Cl2
2Fe2+ + 4Br-+3Cl2= 2Br2+ 6Cl-+2Fe3+
B.硫酸铜溶液中通入硫化氢气体:Cu2+ +H2S = CuS↓+2 H+
C.碳酸氢铵溶液中加入少量氢氧化钠溶液:NH4+十OH- = NH3·H2O
D.以石墨为电极电解CuSO4溶液:2Cu2++
2H2O 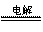 2Cu↓ + O2↑+ 4H+
2Cu↓ + O2↑+ 4H+
12.常见的非极性分子、最外层8e-稳定结构的微粒有许多,下列既属于非极性分子,又属于各原子达8e-稳定结构的分子是:
A.COCl2 B.PCl5 C.SCl2 D.CCl4
11.下列各图所示装置的气密性检查中,漏气的是:
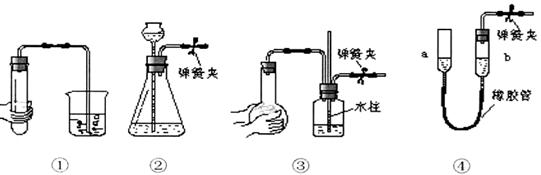
A.对装置①,双手移去后.导管中水面高于烧杯内水面
B.对装置②,长颈漏斗内液面高度保持不变
C.对装置③,长导管内形成一段水柱
D.对装置④,上下移动a管后,a、b两端液面仍相平
10.实验桌上放有托盘天平、研钵、三脚架、泥三角、蒸发皿、坩埚、干燥器、酒精灯、火柴、烧杯、量筒、100 mL容量瓶、药匙、玻璃棒、石棉网、胶头滴管、坩埚钳。从缺乏仪器和用具的角度来看,不能进行的实验项目是:
A.配制0.1 mol / L 100 mL的CuSO4溶液 B.蒸发
C.测定硫酸铜晶体中结晶水的含量 D.萃取 分液
9.海藻中含有丰富的、以离子形式存在的碘元素。下图是实验室从海藻里提取碘的流程的一部分。
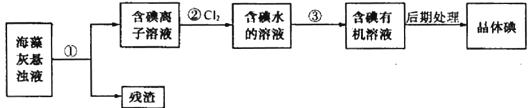
下列判断不正确的是:
A.步骤①、③的操作分别是过滤、萃取
B.为使I- → I2 , 步骤② 中Cl2应适量
C.可用淀粉溶液检验步骤②的反应是否进行完全
D.步骤③中加入的有机溶剂可以是CCl4
8.下列对物质用途的描述中,错误的是:
A.与Mg 、Al 比较,镁铝合金的强度和硬度均较大,常用作航天器的材料
B.Cl2、SO2、NaClO 均可用于漂白某些物质
C.浓硫酸具有吸水性,可用于干燥HCl、H2S、O2
D.二氧化硅、碳酸钠、碳酸钙可用于制玻璃
7.下图为周期表中短周期的一部分。若a原子最外层电子数比次外层电子数少3 ,下列说法正确的是:
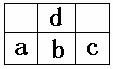
A.只有a 和d 的单质有同素异形体
B.原子半径大小顺序是c> b > a> d
C.b和d 的原子可构成带3 个负电荷的阴离子
D.a、b 、c 最高价氧化物对应水化物酸的强弱关系是c > b > a
6.下列离子组中,能大量共存且无色透明是:
A.c(H +) = 10-13mol · L-1的溶液:Na+、CO32-、S2-、SO32-
B.pH = 0的溶液:Fe3-、NO3-、SO42-、I-
C.pH = 14的溶液:Na+、Ca2+、NO3-、Cl-
D.使紫色石蕊试液变红的溶液:K+、Na+、Ca2+、HCOO-
5.设NA为阿伏加德罗常数,下列叙述不正确的是:
A.60g SiO2含的Si-O键数为4NA
B.标准状况下,22.4L 氮气和氦气所含的原子数相同
C.NH3既易液化,又极易溶于水,都是形成氢键的缘故
D.室温下,42g 乙烯与丙烯的混合气体中含碳原子数为3NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com