
19£®(9·Ö)
ÓŠA”¢B”¢C”¢D”¢E”¢F”¢G 7Ęæ²»Ķ¬ĪļÖŹµÄČÜŅŗ£¬ĖüĆĒø÷ŹĒKCl”¢MgCl2”¢Na2SO4”¢Na2CO3”¢AgNO3”” Ca(NO3)2”¢Ba(OH)2ČÜŅŗÖŠµÄŅ»ÖÖ”£ĪŖĮĖ¼ų±š£¬ø÷ȔɣĮæČÜŅŗ½ųŠŠĮ½Į½»ģŗĻ£¬ŹµŃé½į¹ūČē±ķĖłŹ¾”£±ķÖŠ”°”ż”±±ķŹ¾Éś³É³Įµķ»ņĪ¢ČÜ»ÆŗĻĪļ£¬”°Ņ»”±±ķŹ¾¹Ū²ģ²»µ½Ć÷ĻŌ±ä»Æ”£ŹŌ»Ų“šĻĀĆęĪŹĢā£ŗ

(1)AµÄ»ÆѧŹ½ŹĒ”””””” £¬GµÄ»ÆѧŹ½ŹĒ”””””””” ”£ÅŠ¶ĻĄķÓÉŹĒ”” ”””” ”””””””””””””£
(2)Š“³öĘäÓą¼øÖÖĪļÖŹµÄ»ÆѧŹ½£ŗ
B”””””” ”” ””””C”””” ”””” ”””” ””D”””” ”””” ””E”” ”””” ””””F”””” ”””””” ”£
18£®(11·Ö)
(1)ÓÉ”°C(ŹÆÄ«)== C(½šøÕŹÆ)£»”÷H= +119 kJ/mol ”±æÉÖŖ½šøÕŹÆ±ČŹÆÄ«”””””””” (Ģī”°ĪČ¶Ø”±»ņ”°²»ĪČ¶Ø”±)
(2)ŌŚĻ”ČÜŅŗÖŠ£ŗ H++OH££½H2O£»·Å³öČČĮæ57.3kJ£¬ŌņĻ”ĮņĖįÓėĻ”ĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦µÄÖŠŗĶČȵÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗ
”””” ”””””””””””””””””””””””””””””””””””””””” ”””””””””””””””””””””””£
(3)ėĀ(N2H4)ÓÖ³ĘĮŖ°±£¬ŹĒŅ»ÖÖæÉČ¼ŠŌµÄŅŗĢ壬æÉÓĆ×÷»š¼żČ¼ĮĻ”£ŅŃÖŖŌŚ101kPaŹ±£¬32.0gN2H4ŌŚŃõĘųÖŠĶźČ«Č¼ÉÕÉś³ÉµŖĘų£¬·Å³öČČĮæ624kJ(25”ꏱ)£¬N2H4ĶźČ«Č¼ÉÕ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ŹĒ
”” ”””””””””””””””””””””””””””””””””””””””””” ”””””””””””””””””””””””£
(4)“«Ķ³ÖʱøėĀµÄ·½·Ø£¬ŹĒŅŌNaClOŃõ»ÆNH3£¬ÖʵĆėĀµÄĻ”ČÜŅŗ”£øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ”””””””””””””””””””””””””” ”””””””””””””””””””””””””””””””””£
17£®(12·Ö)w
A”¢B”¢C”¢D”¢EŹĒŗĖµēŗÉŹżŅĄ“ĪŌö“óµÄ5ÖÖ¶ĢÖÜĘŚÖ÷×åŌŖĖŲ£»Ō×Ó°ė¾¶°“D”¢E”¢B”¢C”¢AĖ³ŠņŅĄ“Ī¼õŠ”£¬BŗĶEŹĒĶ¬Ö÷×åŌŖĖŲ”£
(1)ĻĀĮŠĶʶĻÕżČ·µÄŹĒ”” ””””””””
(a)A”¢B”¢E²»æÉÄÜŌŚĶ¬Ņ»Ö÷×å”””””” ””(b)A”¢B”¢CæÉÄÜŌŚĶ¬Ņ»ÖÜĘŚ
(c)CµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļæÉÄÜĻŌ¼īŠŌ ””(d)CŗĶDµÄµ„ÖŹæÉÄÜÉś³ÉĄė×Ó»ÆŗĻĪļ”£
(2)ČōAÓėDĶ¬Ö÷×壬BŹĒŠĪ³É»ÆŗĻĪļÖÖĄą×ī¶ąµÄŌŖĖŲ£¬CŌ×ÓµÄ×īĶā²ćµē×ÓŹż±ČAÓėBµÄ×īĶā²ćµē×Ó×ÜŹż»¹¶ą1”£ŌņAÓėCŌŖĖŲ°“Ō×ÓøöŹż±Č1:1ŠĪ³ÉµÄ»ÆŗĻĪļFµÄµē×ÓŹ½ĪŖ”””””””””””” £»CÓėDŠĪ³ÉµÄŌ×ÓøöŹż±ČĪŖ1:1µÄ»ÆŗĻĪļ19.5gÓė×ćĮæµÄĖ®·“Ó¦Ź±£¬×ŖŅʵē×ÓµÄĪļÖŹµÄĮæĪŖ”””” mol”£
(3)ÓÉABCDĖÄŌŖĖŲŠĪ³ÉµÄĪŽ»ś»ÆŗĻĪļĖ®ČÜŅŗ³Ź”””””””” ŠŌ(ĢīĖį»ņ¼ī)£¬ĘäŌŅņÓĆĄė×Ó·“Ó¦·½³ĢŹ½ĪŖ”””””””””””””””””””””””””””””” ”£
16£®Ķس£ČĖĆĒ°Ń²šæŖ1 molij»Æѧ¼üĪüŹÕµÄÄÜĮæ擳ÉøĆ»Æѧ¼üµÄ¼üÄÜ”£¼üÄܵēóŠ”æÉŅŌŗāĮæ»Æѧ¼üµÄĒæČõ£¬Ņ²æÉŅŌ¹Ą¼Ę»Æѧ·“Ó¦µÄ·“Ó¦ČČ(¦¤H)£¬»Æѧ·“Ó¦µÄ¦¤HµČÓŚ·“Ó¦ÖŠ¶ĻĮŃ¾É»Æѧ¼üµÄ¼üÄÜÖ®ŗĶÓė·“Ó¦ÖŠŠĪ³ÉŠĀ»Æѧ¼üµÄ¼üÄÜÖ®ŗĶµÄ²ī”£ĻĀĮŠŹĒŅ»Š©»Æѧ¼üµÄ¼üÄÜ”£
|
»Æѧ¼ü |
C-H |
C-F |
H-F |
F-F |
¼üÄÜ/(kJ”¤mol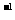 ) ) |
414 |
489 |
565 |
155 |
øł¾Ż¼üÄÜŹż¾Ż¹ĄĖćĻĀĮŠ·“Ó¦µÄ·“Ó¦ČȦ¤HĪŖ£ŗCH4 (g)+4F2 (g) £½CF4+4HF(g)
A£®ØC1940 kJ ”¤ mol£1”””””””””””””” ”””””” B£®1940 kJ ”¤ mol£1
C£®ØC485 kJ ”¤ mol£1”””””””””””””””””””” D£®485 kJ ”¤ mol£1
µŚII¾ķ””Ö÷¹Ū¾ķ(¹²52·Ö)
15£®ĒāŃõ»ÆøĘŌŚ80”ꏱµÄČܽā¶ČĪŖa g£¬ŌŚ20”ꏱµÄČܽā¶ČĪŖb g”£Č”80”ꏱµÄĒāŃõ»Æøʱ„ŗĶČÜŅŗw gÕō·¢µōm gĖ®ŗó£¬ŌŁĄäČ“ÖĮ20”ę£¬“ĖŹ±ČÜŅŗÖŠČÜÖŹµÄÖŹĮæ·ÖŹżĪŖc%£¬ŌņĻĀĮŠ¹ŲĻµŹ½ÖŠÕżČ·µÄŹĒ
A£®a£¾b£¾c”””” ”” ””B£®b£¾a£¾c ””””””””C£®b£¼a£¬b£¼c”” ””””D£®b£¾a£¬b£¾c
14£®ŌŚĻĀĮŠČÜŅŗÖŠ£¬ø÷×éĄė×ÓŅ»¶ØÄܹ»“óĮæ¹²“ęµÄŹĒ
A£®Ź¹·ÓĢŖŹŌŅŗ±äŗģµÄČÜŅŗ£ŗ Na+”¢Cl-”¢SO42-”¢Fe3+
B£®Ź¹×ĻÉ«ŹÆČļŹŌŅŗ±äŗģµÄČÜŅŗ£ŗFe2+”¢Mg2+”¢NO3-”¢Cl-
C£®c(H+)=10-12 mol”¤L-1µÄČÜŅŗ£ŗK+”¢Ba2+”¢Cl-”¢Br-
D£®Ģ¼ĖįĒāÄĘČÜŅŗÖŠ£ŗK+”¢SO42-”¢Cl-”¢H+
13£®Ņ»¶ØĢõ¼žĻĀ£¬ÓĆ¼×ĶéæÉŅŌĻū³żµŖŃõ»ÆĪļ(NOx)µÄĪŪČ¾”£ŅŃÖŖ£ŗ
¢Ł CH4 (g)+4NO2 (g)=4NO (g) +CO2 (g)+2H2O (g) £»”÷H£½ØD574 kJ”¤mol£1
¢Ś CH4 (g)+4NO (g)=2N2 (g)+CO2 (g)+2H2O (g)”” £»”÷H£½ØD1160 kJ”¤mol£1
ĻĀĮŠŃ”ĻīÕżČ·µÄŹĒ
A£®CH4 (g)+2NO2 (g)= N2 (g)+CO2 (g)+2H2O (l) £»”÷H£½ØD867 kJ”¤mol£1
B£®Čō0.2 mol CH4»¹ŌNO2ÖĮN2£¬ŌŚÉĻŹöĢõ¼žĻĀ·Å³öµÄČČĮæĪŖ287 kJ
C£®1molCH4“߻ƻ¹ŌNOxĪŖN2µÄ¹ż³ĢÖŠ£¬Čōx=1.6£¬Ōņ×ŖŅʵĵē×ÓĪŖ3.2 mol
D£®ČōÓƱź×¼×“æöĻĀ2.24L CH4»¹ŌNO2ÖĮN2£¬Õūøö¹ż³ĢÖŠ×ŖŅʵĵē×ÓĪŖ0.8 mol
12£®”°ÉńÖŪĮłŗÅ”±ĖłÓƶÆĮ¦Č¼ĮĻÖ®Ņ»ĪŖĒā»Æļ®ČżŠÖµÜ£ŗLiH”¢LiD”¢LiT”£ĘäÖŠLiµÄÖŹĮæŹżĪŖ7£¬ÓŠ¹ŲĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ
A£®ČżÖÖĪļÖŹÖŹ×ÓŹżÖ®±ČĪŖ1£ŗ2£ŗ3”””””””” ”” ”” B£®ČżÖÖĪļÖŹÖŠ×ÓŹżÖ®±ČĪŖ1£ŗ1£ŗ1
C£®ČżÖÖĪļÖŹµÄĦ¶ūÖŹĮæÖ®±ČĪŖ8£ŗ9£ŗ10 ”” ”” D£®ČżÖÖĪļÖŹµÄ»ÆѧŠŌÖŹ²»ĻąĶ¬
11£®ŌŚÅØŃĪĖįÖŠH3AsO3ÓėSnCl2·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ
SnCl2+Cl£+H3AsO3+H+£As+SnCl62£+M(Ī“ÅäĘ½)£¬¹ŲÓŚøĆ·“Ó¦µÄĖµ·ØÖŠÕżČ·µÄ×éŗĻŹĒ
¢ŁŃõ»Æ¼ĮŹĒH3AsO3 ¢Ś»¹ŌŠŌ£ŗCl££¾As ¢ŪĆæÉś³É0.1molµÄAs£¬»¹Ō¼ĮŹ§Č„µÄµē×ÓĪŖ0.3mol ¢ÜMĪŖOH£ ¢ŻSnCl62£ŹĒŃõ»Æ²śĪļ ¢ŽH+Ē°ĆęµÄÅäĘ½ĻµŹżĪŖ6
A£®¢Ł¢Ū¢Ż¢Ž”””””” ”””””””””””””””””””””””””””” B£®¢Ł¢Ś¢Ü¢Ż””””””””
C£®¢Ł¢Ś¢Ū¢Ü”””””” ”””””””””””””””””””””””””””””” D£®Ö»ÓŠ¢Ł¢Ū¢Ž
10£®ĻĀĮŠĄė×Ó·½³ĢŹ½ÕżČ·µÄŹĒ
A£®½«0.1mol/L HClČÜŅŗŹżµĪ»ŗ»ŗµĪČė1mol/L 50mL Na3PO4ČÜŅŗÖŠ£¬ĒŅ²»¶Ļ½Į°č””
3H++PO43££½H3PO4
B£®½«1mol/L NaAlO2ČÜŅŗŗĶ1.5mol/LµÄHClČÜŅŗµČĢå»ż»„Ļą¾łŌČ»ģŗĻ
6AlO2£+9H++3H2O£½5Al(OH)3”ż+Al3+
C£®Ļņ1mol/LĆ÷·ÆČÜŅŗ50mLÖŠµĪČėŹżµĪ0.1mol/L Ba(OH)2ČÜŅŗ
Al3++2SO42£+2Ba2++3OH££½Al(OH)3”ż+2BaSO4”ż
D£®½«ÉŁĮæSO2ĘųĢåĶØČėNaClOČÜŅŗÖŠ£ŗSO2+H2O+ClO££½SO42£+Cl£+2H+
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com