
20£Æ(10∑÷)Œ“π˙µ⁄∂˛¥˙…Ì∑ð÷§≤…”√µƒ «æþ”–¬Ã…´ª∑±£–‘ƒÐµƒPETG–¬≤ƒ¡œ£¨PETG–¬≤ƒ¡œø…“‘ªÿ ’‘Ÿ¿˚”√£¨∂¯«“∂‘÷бþª∑æ≥≤ªππ≥…»Œ∫ŒŒ€»æ°£’‚“ª≤ƒ¡œ «”…Ω≠À’ª™–≈ÀГµ∑¢’π”–œÞπ´Àæ◊Ó–¬—–∑¢≥…𶵃–¬≤ƒ¡œ£¨≤¢≥…Œ™π´∞≤≤ø∂®µ„≤˙µÿ°£PETGµƒΩ·ππºÚ ΩŒ™£∫
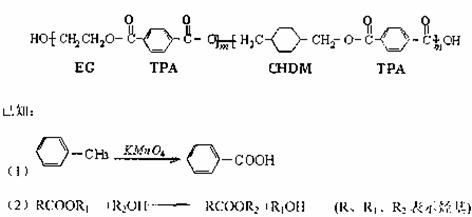
’‚÷÷≤ƒ¡œø…≤…”√“‘œ¬∫œ≥…¬∑œþ£∫
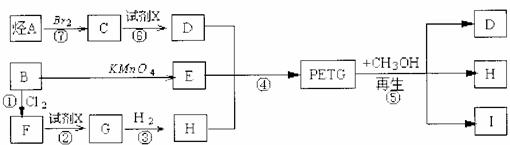
‘ªÿ¥œ¬¡–Œ £∫
°° (1)∑¥”¶¢⁄¢Þº”»Îµƒ ‘º¡x «°°°°°°°°°°°°°°°°°° °£
°° (2)¢ðµƒ∑¥”¶¿ý–Õ «°°°°°°°°°°°°°°°°°° °£
°° (3)–¥≥ˆΩ·ππºÚ Ω£∫B°°°°°°°°°°°°°°°°°° I°°°°°°°°°°°°°°°°°° °£
°° (4)∫œ≥… ±”¶øÿ÷∆µƒµ•ÃµƒŒÔ÷ µƒ¡ø
°°°°°°°° n(D)£∫n(E)£∫n(H)£∫°°°°°°°° £∫°°°°°°°° £∫°°°°°°°° (”√m°¢n±Ì æ)
°° (5)–¥≥ˆªØ—ß∑Ω≥Ã Ω£∫
∑¥”¶¢€£∫°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
∑¥”¶¢Þ£∫°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
19£Æ(13∑÷)ªÿ¥œ¬¡–Œ Â

°° (1)‘⁄…œ±Ì÷–”√ µœþ≤π»´÷Ð∆⁄±Ìµƒ±þΩÁ°£
°° (2)‘™Àÿ¢€°¢¢Ð–Œ≥…µƒ«‚ªØŒÔ»€∑–µ„∏þµƒ «°°°°°°°°°°°°°°°°°° (”√«‚ªØŒÔµƒªØ—ß Ω±Ì æ)‘≠“Ú «°°°°°°°°°°°°°°°°°° °£”√∑¥”¶∑Ω≥à Ω÷§√˜¢€°¢¢ðµƒ∑«Ω Ù–‘«ø»ı°°°°°°°°°°°°°°°°°° °£
°° (3)A°¢B¡Ω÷÷ªØ∫œŒÔæ˘”…¢Ÿ¢⁄¢€¢ÐÀƒ÷÷‘™Àÿ◊È≥…£¨–¥≥ˆ¥À¡Ω÷÷ªØ∫œŒÔ‘⁄ÀƻГ∫÷–∑¢…˙∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω°°°°°°°°°°°°°°°°°° °£
°° (4)¢Ðµ•÷ ‘⁄ø’∆¯÷–»º…’…˙≥…x£¨“—÷™“ª∂®Ãıº˛œ¬16gX±ª—ı∆¯—ıªØ∑≈≥ˆ24£Æ5KJ»»¡ø£¨ –¥≥ˆX»º…’µƒ»»ªØ—ß∑¥”¶∑Ω≥Ã Ω°°°°°°°°°°°°°°°°°° °£
°° (5)‘™Àÿ÷Ð∆⁄±Ì÷–Œª÷√œýΩ¸æÕª·”–ƒ≥–©œýÀ∆µƒ–‘÷ £¨»Á¢Þ°¢¢þ¡Ω‘™Àÿ“≤”–“ª–©œýÀ∆µƒªØ—ß–‘÷ £¨«Î柿˝Õ…√˜¢Þ°¢¢þ‘™ÀÿµƒœýÀ∆–‘(”√ªØ—ß∑Ω≥Ã Ω±Ì æ)£∫°°°°°°°°°°°°°°°° °£
°° (6)œ¬Õº «∏þ÷–ªØ—ßøŒ±æ÷–µƒ µ—È◊∞÷√Õº°£
°°°°°°°° a”√‘™Àÿ∑˚∫≈±Í≥ˆÃ˙‘⁄÷Ð∆⁄±Ì÷–µƒœý”¶Œª÷√°£
°°°°°°°° b◊∞÷√B÷–”–πÿ∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™°°°°°°°°°°°°°°°° °£
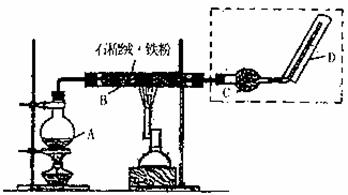
°°°°°°°° cΩ´¢⁄°¢¢€¡Ω‘™Àÿ–Œ≥…µƒ∫¨∑«º´–‘π≤º€º¸µƒªØ∫œŒÔÕ∂»Î¬»ªØ—«Ã˙»Ð“∫÷–£¨ª·¡¢º¥π€≤ϵΩ∫Ï∫÷…´≥¡µÌ£¨Õ¨ ±”–ŒÞ…´∆¯≈ð°£–¥≥ˆ∫Ï∫÷…´≥¡µÌ”Î∆¯Ã «2£∫1 ±µƒ¿Î◊”∑Ω≥Ã Ω£∫°°°°°°°°°°°°°°°°°° °£
17£Æ(5∑÷)«Ë(CN)2µƒªØ—ß–‘÷ ”ά±Àÿ∫ÐœýÀ∆(X2)£¨≥∆Œ™ƒ‚¬±Àÿ°£«ËƒÐ∫Õ«‚∆¯∑¥”¶…˙≥…HCN£¨∆‰ÀƻГ∫ «“ª÷÷À·°£«Ëµƒ—ıªØ–‘±»‰Â»ı£¨±»µ‚«ø°£
°° (1)HCN∑÷◊”÷–∫¨”–4∏ˆπ≤º€º¸£¨–¥≥ˆHCNµƒΩ·ππ Ω
°° (2)KCN»Ð“∫œ‘ºÓ–‘£¨‘≠“Ú «(”√¿Î◊”∑Ω≥Ã Ω±Ì æ)°°°°°°°°°°°°
°° (3)œ¬¡–”–πÿ∑Ω≥à Ω≤ª’˝»∑µƒ «°°°°°°°°°°°° °£
A£Æ(CN)2+2NaOH=NaCN+NaCNO+H2O
B£ÆMnO2+4HCN Mn(CN)2+(CN)2+2H2O
Mn(CN)2+(CN)2+2H2O
°°°°°°°° C£ÆI 2+2KCN=2KI+(CN)2
°°°°°°°° D£ÆœÚNaBraq∫ÕKCNaq÷–º”»Î…Ÿ¡øCl 2£∫Cl 2+2NaBr=2NaCl+Br2
°° (4)¥¶¿ÌCNµƒπ§“µ∑œÀÆ≥£”√C10-—ıªØ¥¶¿Ì…˙≥…CNO-°£∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω»Áœ¬£∫
°°°°°°°° a CN-+bC1O-+2 cOH-=d CNO-+e N2+fCO32-+b Cl-+c H2O
…œ ˆªØ—ß∑Ω≥à Ωø…ƒÐµƒ≈‰∆Ωœµ ˝”–∂ý◊È°£
¢Ÿ∑Ω≥à Ω÷–e:fµƒ÷µŒ™°°°°°°°°°°°° °£
°°°°°°°° A£Æ1°°°° °°°°°°°°°° B£Æ1£Ø2 °°°°°°°°°°°°°° C£Æ2°°°° °°°°°°°°°°°°°°°° D£Æ≤ªƒÐ»∑∂®
¢⁄»Ùd=e=1£¨‘Úb=°°°°°°°°°°°° °£
16£Æ(6∑÷)≥£Œ¬œ¬”–≈®∂»æ˘Œ™0£Æ5m01£ØLµƒÀƒ÷÷»Ð“∫£∫¢ŸNa2CO3£ª¢⁄NaHCO3£Æ¢€HC1¢ÐNa3°§H2O
°° (1)…œ ˆ»Ð“∫÷–£¨ø…∑¢…˙ÀÆΩ‚µƒ «°°°°°°°°°°°° (ÃÓ–Ú∫≈£¨œ¬Õ¨)°£
°° (2)…œ ˆ»Ð“∫÷–£¨º»ƒÐ”Ϋ‚—ıªØƒ∆∑¥”¶£¨”÷ƒÐ∫Õ¡ÚÀ·∑¥”¶µƒ»Ð“∫÷–¿Î◊”≈®∂»¥ÛµΩ–°µƒÀ≥–ÚŒ™°°°°°°°°°°°° °£
°° (3)œÚ»Ð“∫¢Ð÷–º”»Î…Ÿ¡ø¬»ªØÔßπÃ㨥À ±c(NH4+)£Øc(OH-)µƒ÷µ°°°°°°°°°°°° (ÃÓ‘ˆ¥Û°¢ºı–°°¢≤ª±‰)°£
°° (4)»ÙΩ´¢€∫բеƒ»Ð“∫ªÏ∫œ∫ۻГ∫«°∫√≥ ÷––‘£¨‘ÚªÏ∫œ«∞¢€µƒÃª˝°°°°°°°°°°°° ¢ÐµƒÃª˝(ÃÓ¥Û”⁄°¢–°”⁄°¢µ»”⁄)£¨¥À ±»Ð“∫÷–¿Î¡À≈®∂»”…¥ÛµΩ–°µƒÀ≥–Ú «°°°°°°°° °°°°°£
°° (5)»°10mL»Ð“∫¢€£¨º”ÀÆœ° ÕµΩ500mL°££¨‘Ú∏√»Ð“∫÷–”…ÀƵÁ¿Î≥ˆµƒc(H+)=°°°°°°°°°°°° °£
15£ÆΩ´11£Æ9gMg-A1 ®C Fe◊È≥…µƒ∫œΩ»Ð”⁄◊„¡øµƒNaOH»Ð“∫÷–£¨∫œΩ÷ ¡øºı…Ÿ2£Æ7g°£¡Ì»°µ»÷ ¡øµƒ∫œΩ»Ð”⁄π˝¡øœ°œıÀ·÷–£¨…˙≥…6£Æ72L(±Í◊º◊¥øˆ)NO£¨œÚ∑¥”¶∫Ûµƒ»Ð“∫÷–º”»Î ¡øNaOH»Ð“∫«°∫√ πMg2+°¢A13+°¢Fe3+ÕÍ»´◊™ªØŒ™≥¡µÌ£¨‘Ú≥¡µÌ÷ ¡øŒ™(°°°° )
°°°°°° A£Æ22.1°°°°°°°°°°°°°°°°°°°° B£Æ27.2°°°°°°°°°°°°°°°°°°°° C£Æ30°°°° °°°°°°°°°°°°°° D£ÆŒÞ∑®»∑∂®
µ⁄¢ÚæÌ(∑«—°‘Ò°° π≤55∑÷)
14£Æ µ—È ““ª∆øπÃÃÂMµƒ±Í«©”“∞Î≤ø∑÷“—±ª∏Ø ¥£¨ £”ý≤ø∑÷÷ªø¥µΩ°∞NazS°±◊÷—˘°£“—÷™πÃÃÂM÷ªø…ƒÐ «Na2S°¢Na2SO3°¢ Na2SiO4°¢Na2SO4°¢Na2S2O3÷–µƒ“ª÷÷°£»Ù»°…Ÿ¡øπÃÃÂM≈‰≥…»Ð“∫Ω¯––”–πÿ µ—È£¨œ¬¡–Àµ∑®÷–≤ª’˝»∑µƒ «°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° (°°°° )
°°°°°° A£ÆœÚ»Ð“∫÷–º”œ°œıÀ·À·ªØµƒBaC12£¨»Ù”–∞◊…´≥¡µÌ£¨‘ÚπÃÃÂMŒ™Na2SO4
°°°°°° B£ÆœÚ»Ð“∫÷–Õ®»ÎCO2£¨»Ù”–∞◊…´≥¡µÌ£¨‘ÚπÃÃÂMŒ™Na2SiO3
°°°°°° C£Æ”√pH ‘÷ΩºÏ—È£¨»ÙpH=7‘ÚπÃÃÂM“ª∂® «Na2SO4
°°°°°° D£Æ÷ª”√—ŒÀ·“ª÷÷ ‘º¡æÕø…“‘»∑∂®∏√πÃÃÂMµƒæþÃÂ≥…∑÷
13£Æœ¬¡–πÿ”⁄Àƒ∏ˆÕºœÒµƒÀµ∑®’˝»∑µƒ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° (°°°° )
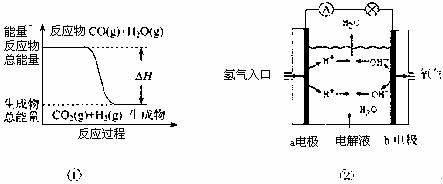
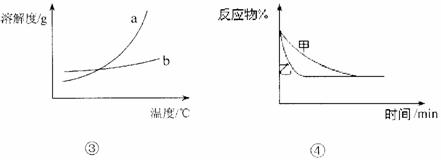
°°°°°° A£ÆÕº¢Ÿ±Ì æªØ—ß∑¥”¶÷–ƒÐ¡øµƒ±‰ªØ£¨∑¥”¶CO(g)+H2O(g)=CO2(g)+H2(g)µƒ°˜H>0
°°°°°° B£ÆÕº¢⁄Œ™«‚—ı»º¡œµÁ≥ÿ æ“‚Õº£¨’˝°¢∏∫º´Õ®»Îµƒ∆¯ÃÂê˝÷Ʊ»Œ™2£∫1
°°°°°° C£ÆÕº¢€±Ì æŒÔ÷ a°¢bµƒ»ÐΩ‚∂»«˙œþ£¨ø…“‘”√Ω·æß∑Ω∑®¥”a°¢bªÏ∫œŒÔ÷–÷¥øa
°°°°°° D£ÆÕº¢Ðø…“‘±Ì æ—π«ø∂‘ø…ƒÊ∑¥”¶2A(g)+2B(g)°°°° °°3C(g)+D(s)µƒ”∞œÏ£¨«“““µƒ—π«ø¥Û
12£Æœ¬¡–»Ð“∫÷–”–πÿŒ¢¡£µƒŒÔ÷ µƒ¡ø≈®∂»πÿœµ’˝»∑µƒ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° (°°°° )
°°°°°° A£ÆNaHSO3∫ÕNaHCO3µƒ÷––‘ªÏ∫œ»Ð“∫÷–(HSO3-∫ÕHCO3-æ˘R”√±Ì æ)£∫
°°°°°°°°°°°°°° c(Na+)=c(HRO3-)+2c(RO32-)
°°°°°° B£Æ≥£Œ¬œ¬Ω´¥◊À·ƒ∆°¢—ŒÀ·¡Ω»Ð“∫ªÏ∫œ∫Û£¨»Ð“∫≥ ÷––‘£¨‘ÚªÏ∫œ∫ۻГ∫÷–£∫
°°°°°° c(Na+)>c(Cl-)>c(CH3COO-)
°°°°°° C£Æ≥£Œ¬œ¬ŒÔ÷ µƒ¡ø≈®∂»œýµ»µƒ¢Ÿ(NH4)2CO3°¢°° ¢⁄(NH4)3SO4°¢ ¢€(NH4)2Fe(SO4)2»˝÷÷»Ð“∫÷–c(NH4+)£∫¢€>¢Ÿ>¢⁄
°°°° D£Æµ»Ãª˝µ»ŒÔ÷ µƒ¡ø≈®∂»µƒNaC1O”ÎNaCl»Ð“∫÷–¿Î◊”◊Ð ˝∂ý…Ÿ£∫N(NaClO)>N(NaCl)
11£Æœ¬ÕºŒ™‘™Àÿ÷Ð∆⁄±Ì∂Ã÷Ð∆⁄µƒ“ª≤ø∑÷£¨œ¬¡–”–πÿA°¢B°¢C°¢DÀƒ÷÷‘™Àÿµƒ– ˆ÷–’˝»∑µƒ «(°°°° )
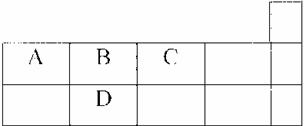
°°°°°° A£Æ‘≠◊”∞Îæ∂¥Û–°±»ΩœŒ™A>B>C>D
°°°°°° B£ÆA°¢B°¢C°¢Dµƒµ•÷ ‘⁄≥£Œ¬œ¬æ˘≤ªµºµÁ
°°°°°° C£Æ…˙≥…«‚ªØŒÔµƒŒ»∂®–‘A>B>C>D
°°°°°° D£ÆA”ÎC–Œ≥…µƒ“ı¿Î◊”ø…ƒÐ”–AC32-°¢A2C42-
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com