
25£Æ(5∑÷)œÚWg”…NaHS°¢Na2SO3 °¢CuSO4◊È≥…µƒªÏ∫œŒÔ÷–£¨º”»Î“ª∂®¡øµƒÀÆ≥‰∑÷∑¥”¶∫Ûπ˝¬À°£¬À“∫÷–÷ª∫¨”–Na2SO4£¨¬À‘¸≤ª»Ð”⁄œ°—ŒÀ·£¨«“∑¥”¶π˝≥Ã÷–ŒÞ∆¯Ã“ð≥ˆ°£(“—÷™£∫∞—H2SÕ®»ÎCuSO4»Ð“∫÷–ª·∑¢…˙œ¬¡–∑¥”¶£∫H2S+CuSO4=H2SO4+CuS°˝)
(1)¬À‘¸µƒ≥…∑÷ «___________°£
(2)‘≠ªÏ∫œŒÔ÷–NaHS°¢Na2SO3°¢CuSO4µƒŒÔ÷ µƒ¡ø÷Ʊ» «______________°£
(3)”√¿Î◊”∑¥”¶∑Ω≥Ã Ω±Ì æ¬À‘¸µƒ–Œ≥…π˝≥Ã_____________________________£¨
24£Æ(8∑÷)Ω´Na2CO3∫ÕNaHCO3µƒªÏ∫œŒÔπ≤19øÀ£¨º”»»µΩ÷ ¡ø≤ª‘Ÿ∑¢…˙±‰ªØ ±£¨≥∆µ√ £”ýπÃÃÂ÷ ¡øŒ™15.9øÀ°£‘Ú
°° (1) £”ýπÃà«°°°°°°°° (ªØ—ß Ω)£¨
°° (2)‘≠ªÏ∫œŒÔ÷–Na2CO3µƒŒÔ÷ µƒ¡ø «°°°° mol°£
°° (3)“—÷™Na2CO3∫Õœ°—ŒÀ·∑¥”¶∑÷¡Ω≤ΩΩ¯––£∫
°°°°°°°° Na2CO3+HC1°˙NaC1+NaHCO3°°°°
°°°°°°°° NaHCO3+HC1°˙NaC1+CO2°¸+H2O
°°°°°°°° »ÙΩ´…œ ˆ19gªÏ∫œŒÔ»Ð”⁄ ¡øµƒÀÆ÷–≈‰≥…»Ð“∫£¨‘⁄∏√»Ð“∫÷–÷µŒº”»Î1mol/Lµƒœ°—ŒÀ·£¨”√œ˚∫ƒµƒ—ŒÀ·Ãª˝(mL)◊˜Œ™∫·◊¯±Í£¨∑¥”¶≤˙…˙µƒCO2µƒÃª˝◊˜Œ™◊ð◊¯±Íµ√µΩ»Áœ¬ÕºœÒ£∫
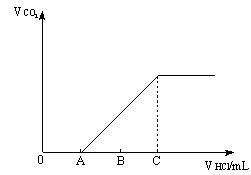
°°°°°°°° «Û£∫Aµ„∂‘”¶»Ð“∫µƒ»Ð÷ «°°°°°°°°°°°°°°°° (Ãѧ Ω)£ªCµ„ ±œ˚∫ƒ—ŒÀ·µƒÃª˝ «°°°°°°°°°°°° mL°£
23£Æ(10∑÷)怱˚œ©ı£∞∑÷˜“™”√”⁄ÀƵƒæªªØ¥¶¿Ì°¢÷ΩΩ¨µƒº”𧵻°£±˚œ©ı£∞∑ «“ª÷÷≤ª±•∫Õı£∞∑£¨ «…˙≤˙怱˚œ©ı£∞∑µƒ‘≠¡œ°£∆‰Ω·ππºÚ ΩŒ™£∫
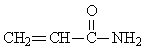
±˚œ©ı£∞∑ø…”…ªØ∫œŒÔA(∑÷◊” ΩC3H6)æ≠º∏≤Ω∑¥”¶÷∆µ√£¨∑¥”¶π˝≥ûÁœ¬£∫
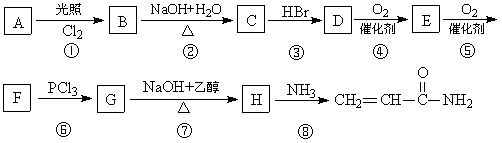
“—÷™£∫(1)3RCOOH+PCl3 3RCOCl+H3PO3
3RCOCl+H3PO3
°°°°°°°°
(2)RCOCl+NH3 RCONH2+HCl
RCONH2+HCl
‘ªÿ¥œ¬¡–Œ £∫
(1)πÿ”⁄±˚œ©ı£∞∑µƒœ¬¡–– ˆ÷–’˝»∑µƒ «£∫°°°°°°°°°°°°°°
°°°°°°°°°° A£ÆƒÐ πÀ·–‘KMnO4»Ð“∫Õ …´£ª°°
B£ÆƒÐ∑¢…˙º”æ€∑¥”¶…˙≥…∏þ∑÷◊”ªØ∫œŒÔ£ª
°°°°°°°°°° C£Æ”ζ¡-∞±ª˘““À·ª•Œ™Õ¨œµŒÔ£ª°°
D£ÆƒÐ”ÎH2∑¢…˙º”≥…∑¥”¶
(2)–¥≥ˆD Eµƒ∑¥”¶∑Ω≥Ã Ω£∫
Eµƒ∑¥”¶∑Ω≥Ã Ω£∫
°°°°°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
(3)C Dµƒƒøµƒ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
£ª…œ ˆ∑¥”¶π˝≥Ã÷– Ù”⁄»°¥˙∑¥”¶µƒ «£∫°°°°°°°°°°
°°°°°°°°°°°°°°°°°°°°°°°°°£
Dµƒƒøµƒ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
£ª…œ ˆ∑¥”¶π˝≥Ã÷– Ù”⁄»°¥˙∑¥”¶µƒ «£∫°°°°°°°°°°
°°°°°°°°°°°°°°°°°°°°°°°°°£
(4)±˚œ©ı£∞∑‘⁄“ª∂®Ãıº˛œ¬ƒÐ∑¢…˙ÀÆΩ‚∑¥”¶£¨ ‘–¥≥ˆ∆‰‘⁄NaOH»Ð“∫÷–ÀÆΩ‚µƒªØ—ß∑Ω≥Ã Ω£∫°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
(5)±˚œ©ı£∞∑”–∂ý÷÷Õ¨∑÷“Ïππã¨Õ¨ ±∑˚∫œœ¬¡–“™«ÛµƒÕ¨∑÷“ÏππÔ–∂ý÷÷£¨ ‘–¥≥ˆ2÷÷£∫
¢Ÿ¡¥◊¥£¨ŒÞúú»˛º¸£ª
¢⁄Õ¨“ª∏ˆÃº‘≠◊”…œ≤ªƒÐÕ¨ ±¡¨”–-NH2∫Õ-OHªÚÀ´º¸∫Õ-NH2(-OH)£ª
¢€Õ¨“ª∏ˆÃº‘≠◊”…œ≤ªƒÐ¡¨”–2∏ˆÀ´º¸°£
°°°°°°°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
22£Æ(10∑÷)N2O5 «“ª÷÷–¬–ÕœıªØº¡£¨∆‰–‘÷ ∫Õ÷∆±∏ ’µΩ»À√«µƒπÿ◊¢°£
°° (1)“ª∂®Œ¬∂»œ¬£¨‘⁄∫„»ð√б’»ð∆˜÷–N2O5ø…∑¢…˙œ¬¡–∑¥”¶£∫
°°°°°°°°°°
2N2O5(g)
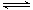 4NO2(g)+O2(g)
£ª®SH£æ0
4NO2(g)+O2(g)
£ª®SH£æ0
°°°° °°°°¢Ÿ»Ù∑¥”¶¥ÔµΩ∆Ω∫‚∫Û£¨Õ®»Î“ª∂®¡øµ™∆¯£¨‘ÚN2O5µƒ◊™ªØ¬ Ω´______(ÃÓ°∞‘ˆ¥Û°±°¢°∞ºı–°°±°¢°∞≤ª±‰°±)°£
°° °°°°°°¢⁄œ¬±ÌŒ™∑¥”¶‘⁄T1Œ¬∂»œ¬µƒ≤ø∑÷ µ—È ˝æð£∫
|
t/s |
0 |
500 |
1000 |
|
c(N2O5)/mol°§L-1 |
5.00 |
3.52 |
2.48 |
°°°°°° ‘Ú500sƒ⁄N2O5µƒ∑÷Ω‚ÀŸ¬ Œ™______________°£
°°°°°° ¢€‘⁄T2Œ¬∂»œ¬£¨∑¥”¶1000s ±≤‚µ√NO2µƒ≈®∂»Œ™4.98mol/L£¨‘ÚT2________T1.
(2)»ÁÕºÀ˘ æ◊∞÷√ø…”√”⁄÷∆±∏N2O5£¨‘ÚN2O5‘⁄µÁΩ‚≥ÿµƒ__________«¯…˙≥…(°∞“ıº´°±ªÚ°∞—Ùº´°±)£¨∆‰µÁº´∑¥”¶ ΩŒ™°°°°°°°°°°°°°°°°°°
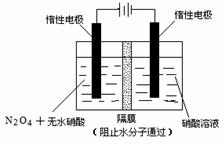
21£Æ(9∑÷) º◊°¢““°¢±˚°¢ŒÏµƒø’º‰Ω·ππ∂º «’˝Àƒ√Ê㨵•÷ º◊∫ÕªØ∫œŒÔ““‘⁄∏þŒ¬œ¬ø…“‘∑¢…˙÷√ªª∑¥”¶£¨±˚°¢∂°°¢ŒÏ»˝÷÷¡£◊”∫¨”–œýÕ¨µƒµÁ◊” ˝£¨ŒÏ «“ª÷÷—Ù¿Î◊”°£∂°‘⁄≥£Œ¬œ¬≥ “∫裨À¸ƒÐµÁ¿Î…˙≥…2÷÷µ»µÁ◊”µƒŒ¢¡£°£
°° (1)–¥≥ˆµ•÷ º◊∫ÕªØ∫œŒÔ““∑¢…˙µƒªØ—ß∑Ω≥Ã Ω°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °°
°° (2)±˚ «ÃÏ»ª∆¯µƒ÷˜“™≥…∑÷£¨±˚∫Õ∂°‘⁄¥þªØ°¢º”»»µƒÃıº˛œ¬£¨ƒÐµ√µΩ2÷÷ø…»º–‘µƒ∆¯Ã£¨–¥≥ˆ∏√ªØ—ß∑Ω≥Ã Ω°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° £¨±˚∫Õø’∆¯ø…◊˜»º¡œµÁ≥ÿ£¨–¥≥ˆ‘⁄ºÓ–‘ΩÈ÷ ÷–∏√µÁ≥ÿµƒ’˝º´∑¥”¶ Ω°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °°°£
°°(3)–¥≥ˆ∂°µÁ¿Î…˙≥…2÷÷µ»µÁ◊”Œ¢¡£µƒµÁ¿Î∑Ω≥Ã Ω°°°°°°°°°°°°°°°°°°°°°°°°°°°°
°° (4) “Œ¬œ¬£¨∫¨”–ŒÏµƒ—Œ»Ð“∫µƒPH°°°°°°°° 7(ÃÓ°∞¥Û”⁄°±°¢°∞–°”⁄°±ªÚ°∞≤ªƒÐ»∑∂®°±)°£
20£Æ(9∑÷)”√œ¬ÕºÀ˘ æ◊∞÷√Ω¯–– µ—È£¨Ω´A÷µŒº”»ÎB÷–£∫
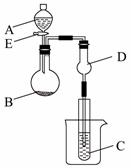
(1)»ÙAŒ™≈®H2SO4£¨BŒ™µ⁄»˝÷Ð∆⁄Ω Ù‘™Àÿµƒµ•÷ £¨∆‰‘⁄≥£Œ¬œ¬ƒ—”ÎÀÆ∑¥”¶£ªCŒ™∆∑∫ϻГ∫£¨ µ—È÷–π€≤ÏµΩ»Ð“∫Õ …´£¨‘ÚB « °°°°°°°°°°°°°°(Ãѧ Ω)£¨B”Î≈®H2SO4»Ð“∫∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™ °°°°°°°°°°°°°°°°°°£ª∑¥”¶∫ÛÕ˘…’±≠÷–º”»Î∑–ÀÆ£¨”÷ø…π€≤쵽 ‘πÐC÷–µƒœ÷œÛŒ™°°°°°°°°°°°° °°°£
(2)»ÙBŒ™Na2CO3£¨CŒ™C6H5ONa»Ð“∫, µ—È÷–π€≤ÏµΩ–° ‘πЃ⁄»Ð“∫±‰ªÎ◊«£¨‘ÚÀ·A”¶æþ”–µƒ–‘÷ «°°°°°°°°°°°°°° °£
»ª∫ÛÕ˘…’±≠÷–º”»Î∑–ÀÆ£¨ø…π€≤쵽 ‘πÐC÷–µƒœ÷œÛ «°°°°°°°°°°°°°°°°°°°°°° °£
(3)»ÙB «…˙ ت“£¨ µ—È÷–π€≤ϵΩC»Ð“∫œ»–Œ≥…≥¡µÌ£¨»ª∫Û≥¡µÌ»ÐΩ‚£¨µ±»Ð“∫«°∫√≥Œ«Â ±£¨πÿ±’E£¨»ª∫ÛÕ˘…’±≠÷–º”»Î»»ÀÆ£¨æ≤÷√∆¨øã¨π€≤쵽 ‘πб⁄≥ˆœ÷π‚¡¡µƒ“¯æµ£¨‘ÚA «°°°°°°°°°°°° (ÃÓ√˚≥∆)£¨C «°°°°°°°° ”Î∆œÃ—뵃ªÏ∫œ“∫£¨“«∆˜D‘⁄¥À µ—È÷–µƒ◊˜”√ «°°°°°°°°°°°°°°°°°°°° °£
19£Æ(3∑÷)œ¬¡–”–πÿ µ—ȵƒ– ˆ£¨’˝»∑µƒ «°°°°°°°°°°°°°°°°°°°°°° °£
°° °°°° A£ÆŒ™¡À≤‚∂®ƒ≥»Ð“∫µƒpH£¨Ω´æ≠ÀÆ»Û ™µƒpH ‘÷ΩΩ˛»ÎµΩ¥˝≤‚»Ð“∫£¨π˝“ªª·»°≥ˆ£¨”αÍ◊º±»…´ø®Ω¯––∂‘±»
°° °°°° B£Æ÷∆““œ© ±£¨Œ¬∂»º∆”¶≤»Î∑¥”¶ªÏ∫œ“∫÷–
°° °°°° C£ÆΩ´Õ≠Àø‘⁄æ∆æ´µ∆…œº”»»∫Û£¨¡¢º¥…ϻΌÞÀÆ““¥º÷–£¨Õ≠Àøª÷∏¥≥…‘≠¿¥µƒ∫Ï…´
°° °°°° D£Æ”√À· ΩµŒ∂®πСø»°20.00mL∏þ√ÃÀ·ºÿ»Ð“∫
°° °°°° E£Æ≈‰÷∆1 mol•L£≠1µƒNaOH»Ð“∫ ±£¨œ¬¡–≤Ÿ◊˜ª·‘Ï≥…À˘≈‰≈®∂»∆´µÕ£∫¢Ÿ»ÐΩ‚∫Û…’±≠Œ¥∂ý¥Œœ¥µ” ¢⁄∂®»ð ±—ˆ ”øÃ∂»œþ ¢€»ð¡ø∆ø÷–‘≠”–…Ÿ–Ì’Ù¡ÛÀÆ
°° °°°° F£Æ÷§√˜µÌ∑€“—ÀÆΩ‚£¨œÚµÌ∑€»Ð“∫÷–º”»Îœ°¡ÚÀ·£¨ÀÆ‘°º”»»“ª∂Œ ±º‰∫Ûº”»Î“¯∞±»Ð“∫£¨ π∆‰∑¢…˙“¯æµ∑¥”¶
°°°°°° G£Æ”√‰ÂÀÆ≥˝»•““œ©÷–ªÏ”–µƒ∂˛—ıªØ¡Ú∆¯ÃÂ
18£Æœ¬¡–Àƒ÷÷»Ð“∫£∫¢ŸpH=2µƒCH3COOH»Ð“∫£ª¢⁄pH=2µƒHCl»Ð“∫£ª¢€pH=12µƒ∞±ÀÆ£ª¢ÐpH=12µƒNaOH»Ð“∫°£œýÕ¨Ãıº˛œ¬£¨”–πÿ…œ ˆ»Ð“∫µƒ±»Ωœ÷–£¨’˝»∑µƒ «°°°° (°°°° )
°°°° A£Æ”…ÀƵÁ¿Îµƒc(H+)£∫¢Ÿ=¢⁄£æ¢€=¢Ð
°°°° B£ÆΩ´¢⁄°¢¢€¡Ω÷÷»Ð“∫ªÏ∫œ∫Û£¨»ÙpH=7£¨‘Úœ˚∫ƒ»Ð“∫µƒÃª˝£∫¢⁄>¢€
°°°° C£Æµ»Ãª˝µƒ¢Ÿ°¢¢⁄°¢¢Ð»Ð“∫∑÷±”Î◊„¡ø¬¡∑€∑¥”¶£¨…˙≥…H2µƒ¡ø£∫¢⁄◊Ó¥Û
°°°° D£ÆœÚµ»Ãª˝µƒÀƒ÷÷»Ð“∫÷–∑÷±º”»Î100mLÀÆ∫Û£¨»Ð“∫µƒpH£∫¢€>¢Ð>¢Ÿ>¢⁄
µ⁄¢ÚæÌ(∑«—°‘Ò°° π≤54∑÷)
17£Æ»‚∂æºÓ «“ª÷÷æþ”–∂ý÷÷…˙¿Ìπ¶ƒÐµƒ∞±ª˘À·¿ýŒÔ÷ £¨”÷√˚Œ¨…˙ÀÿBt£¨ «“ª÷÷¿ýŒ¨…˙Àÿ°£1927ƒÍ≤‚∂®¡ÀÀ¸µƒΩ·ππ£¨1958ƒÍ∑¢œ÷∆‰ƒÐ¥ŸΩ¯÷¨∑æ¥˙–ª£¨1985ƒÍ±ª÷∏∂®Œ™°∞∂ýπ¶ƒÐ”™—¯∆∑°±°£œ¬¡–”–πÿ»‚∂æºÓµƒÀµ∑®≤ª’˝»∑µƒ «£∫°°°°°°°°°°°° (°°°° )
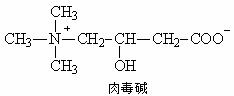
°°°°°° A£Æ»‚∂æºÓµƒ∑÷◊” ΩŒ™£∫C7H15NO3
°° °°°° B£Æ»‚∂æºÓƒÐ”Ϋ‚—ıªØƒ∆∑¥”¶µ´≤ªƒÐ”ΗŒÀ·∑¥”¶
°° °°°° C£Æ“ª∂®Ãıº˛œ¬»‚∂æºÓƒÐ∑¢…˙ı•ªØ∑¥”¶°¢œ˚»•∑¥”¶°¢»°¥˙∑¥”¶
°° °°°° D£Æ»‚∂æºÓƒÐ»Ð”⁄ÀÆ£¨ƒ—»Ð”⁄±Ω
16£Æ»Áœ¬Õº£¨BŒ™≥£º˚Ω ÙªÚ∑«Ω Ùµ•÷ £¨”–œ¬¡–◊™ªØπÿœµ£∫
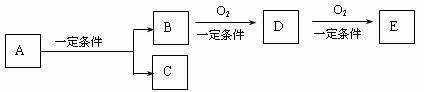
»ÙC «ø…”√◊˜◊‘¿¥ÀÆœ˚∂浃∆¯Ã£¨D°¢E «—ıªØŒÔ£¨D◊™ªØŒ™E ±£¨‘ˆº”—ıµƒ÷ ¡ø‘º «DŒÔ÷ ◊Ð÷ ¡øµƒ25.8%£¨‘ÚA «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° (°°°° )
°° °°°° A£ÆNaCl°°°°°° °°°°°° B£ÆAlCl3°°°°°° °°°° C£ÆH2O2°°°°°° °°°°°° D£ÆKCl
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com