
18£Æ(10∑÷)‘⁄2008ƒÍ≥ıŒ“π˙ƒœ∑Ω‘‚”ˆµƒ±˘—©‘÷∫¶÷–£¨ π”√¡À“ª÷÷»⁄—©º¡£¨∆‰÷˜“™≥…∑÷µƒªØ—ß ΩŒ™XY£¨X°¢Yæ˘Œ™‘™Àÿ÷Ð∆⁄±Ì«∞20∫≈‘™Àÿ£¨∆‰—Ù¿Î◊”∫Õ“ı¿Î◊”∑÷± «10µÁ◊”∫Õ18µÁ◊”µƒµ•∫À¡£◊”£¨«“1molXY∫¨”–28molµÁ◊”°£
¢≈∏√»⁄—©º¡µƒªØ—ß Ω «_______£ªx”Ϋ‚‘™Àÿ–Œ≥…µƒªØ∫œŒÔµƒµÁ◊” Ω «_________°£
¢∆‘™ÀÿD°¢E‘≠◊”µƒ◊ÓÕ‚≤„µÁ◊” ˝ «∆‰µÁ◊”≤„ ˝µƒ2±∂£¨D”ÎYœý¡⁄£¨‘ÚDÀ˘‘⁄Õ¨÷˜◊‘™Àÿµƒ«‚ªØŒÔ÷–£¨∑–µ„◊ÓµÕµƒ «____________(ªØ—ß Ω)£ªEµƒ‘≠◊”Ω·ππ æ“‚Õº «_____°°°° _____°£
¢«‘™ÀÿR”ÎYÕ¨÷˜◊£¨∆‰«‚ªØŒÔƒÐ”√”⁄øà ¥≤£¡ß£¨R2”ÎH2O»Ð“∫∑¥”¶µƒ≤˙ŒÔ÷Æ“ª «O2£¨∏√∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™_______________________________________________°£
17£Æ(7∑÷)(1)1986ƒÍ£¨ªØ—ß…œµ⁄“ª¥Œ”√∑«µÁΩ‚∑®÷∆µ√∑˙∆¯°£ ‘≈‰∆Ω∏√∑¥”¶µƒªØ—ß∑Ω≥Ã Ω£∫
°°°°°° K2MnF6 + °°°°°°SbF5°° =°° KSbF6 +°° MnF3°° + °°°°F2 °°£ª∏√∑¥”¶÷–°°°° ‘™Àÿ±ªªπ‘≠°£
(2)«Ë(CN)2”ΡګË(SCN)2µƒªØ—ß–‘÷ ∫Õ¬±ÀÿœýÀ∆£¨ªØ—ß…œ≥∆Œ™°∞ƒ‚¬±Àÿ°±°£À¸√«“ı¿Î◊”µƒªπ‘≠–‘«ø»ıŒ™£∫Cl£≠<Br£≠<CN£≠<SCN£≠<I£≠°£ ‘–¥≥ˆ£∫
¢Ÿ(CN)2”ÎNaOH»Ð“∫∑¥”¶µƒªØ—ß∑Ω≥Ã Ω£∫°°°°°°°°°°°°°°°°°°°°°°°°°° °£
¢⁄KBr∫ÕKSCNµƒªÏ∫œ»Ð“∫÷–º”»Î(CN)2∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω£∫°°°°°°°°°°°°°°°°°° °£
16£Æœ¬¡–Àµ∑®ªÚ±Ì æ∑®’˝»∑µƒ «
A£Æµ»¡øµƒ∞◊¡◊’Ù∆¯∫Õ∞◊¡◊πÃÃÂ∑÷±ÕÍ»´»º…’£¨∫Û’þ∑≈≥ˆ»»¡ø∂ý
B£Æ”…C( ؃´)°˙C(Ω∏’ Ø)£ª¶§H = +119 kJ°§ mol-1ø…÷™£¨Ω∏’ ر» ؃´Œ»∂®
C£Æ‘⁄œ°»Ð“∫÷–£∫H+(aq)+OH£≠(aq)= H2O(l)£ª¶§H=£≠57.3 kJ°§ mol-1£¨»ÙΩ´∫¨0.5 mol H2SO4µƒ≈®¡ÚÀ·”Î∫¨1 mol NaOHµƒ»Ð“∫ªÏ∫œ£¨∑≈≥ˆµƒ»»¡ø¥Û”⁄57.3 kJ
D£Æ‘⁄101 kPa ±£¨2g H2ÕÍ»´»º…’…˙≥…“∫èÀÆ£¨∑≈≥ˆ285.8 kJ»»¡ø£¨«‚∆¯»º…’µƒ»»ªØ—ß∑Ω≥Ã Ω±Ì æŒ™2H2(g)+O2(g)= 2H2O(l)£ª¶§H=£≠285.8 kJ°§ mol-1
15£Æ“—÷™A°¢B°¢C°¢D°¢E «∫ÀµÁ∫… ˝“¿¥Œ‘ˆ¥ÛµƒŒÂ÷÷∂Ã÷Ð∆⁄‘™Àÿ£¨‘≠◊”∞Îæ∂∞¥D°¢E°¢B°¢C°¢AµƒÀ≥–Ú“¿¥Œºı–°£¨B∫ÕEÕ¨÷˜◊£¨œ¬¡–Õ∆∂œ≤ª’˝»∑µƒ «
A£ÆA°¢B°¢E“ª∂®‘⁄≤ªÕ¨÷Ð∆⁄°°°° °°°°°°°°°° B£ÆDŒ™µ⁄∂˛÷Ð∆⁄
°°°°°° C£ÆA°¢Dø…ƒÐ‘⁄Õ¨“ª÷˜◊°°°°°°°°°°°°°°°° °° °°°°D£ÆC°¢Dµƒµ•÷ ø…ƒÐªØ∫œŒ™¿Î◊”ªØ∫œŒÔ
14£Æ π”√»ð¡ø∆ø≈‰÷∆»Ð“∫ ±£¨”…”⁄≤Ÿ◊˜≤ªµ±£¨ª·“˝∆ŒÛ≤Ó£¨œ¬¡–«Èøˆª· πÀ˘≈‰»Ð“∫≈®∂»∆´µÕµƒ «
¢Ÿ”√ÃÏ∆Ω( π”√”Œ¬Î)≥∆¡ø ±£¨±ª≥∆¡øŒÔ”ÎÌ¿¬ÎµƒŒª÷√∑≈µþµπ¡À
¢⁄”√µŒ∂®πСø»°“∫à±£¨ø™ º ±∆Ω ”∂¡ ˝£¨Ω· ¯ ±∏© ”∂¡ ˝
¢€»Ð“∫◊™“∆µΩ»ð¡ø∆ø∫Û£¨…’±≠º∞≤£¡ß∞ÙŒ¥”√’Ù¡ÛÀÆœ¥µ”
¢Ð◊™“∆»Ð“∫«∞»ð¡ø∆øƒ⁄”–…Ÿ¡ø’Ù¡ÛÀÆ
¢ð∂®»ð ±£¨—ˆ ”»ð¡ø∆øµƒøÃ∂»œþ
¢Þ∂®»ð∫Û“°‘»£¨∑¢œ÷“∫√ÊΩµµÕ£¨”÷≤πº”…Ÿ¡øÀÆ£¨÷ÿ–¬¥ÔµΩøÃ∂»œþ
A£Æ¢Ÿ¢€¢ð¢Þ°°°° °°°°°°B£Æ¢Ÿ¢⁄¢ð¢Þ°°°° °°C£Æ¢⁄¢€¢Ð¢Þ°° °°°°D£Æ¢€¢Ð¢ð¢Þ
13£Æ»ÁÕº‘⁄◊¢…‰∆˜÷–º”»Î…Ÿ¡øNa2SO3æßã¨≤¢Œ¸»Î…Ÿ¡ø≈®¡ÚÀ·°£‘Úœ¬¡–”–πÿÀµ∑®’˝»∑µƒ «
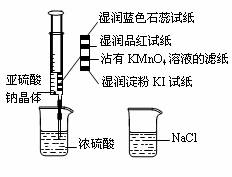
A£Æ¿∂…´ Ø»Ô ‘÷Ωœ»±‰∫Ï∫ÛÕ …´
B£Æ∆∑∫Ï ‘÷Ω∫Õ’¥”–KMnO4»Ð“∫µƒ¬À÷Ωæ˘Õ …´£¨÷§√˜SO2”–∆Ø∞◊–‘
C£Æ ™»ÛµÌ∑€KI ‘÷ΩŒ¥±‰¿∂Àµ√˜SO2µƒ—ıªØ–‘»ı”⁄I2
D£ÆNaCl»Ð“∫ø…”√”⁄≥˝»• µ—È÷–∂ý”ýµƒSO2
12£Æœ¬¡–∑¥”¶¿Î◊”∑Ω≥Ã Ω’˝»∑µƒ «
A£ÆœÚ¬»ªØ¬¡»Ð“∫÷–º”»Îπ˝¡ø«‚—ıªØƒ∆»Ð“∫£∫Al3+ + 4OH- == AlO2- + 2H2O
B£ÆúÀ·«‚ƒ∆»Ð“∫”Îπ˝¡ø ت“ÀÆ∑¥”¶£∫2HCO3£≠+Ca2++2OH£≠£ΩCaCO3°˝+CO32-+2H2O
C£ÆœÚCa(ClO)2»Ð“∫÷–Õ®»Î ¡øSO2 £∫Ca2++2ClO-+SO2+H2O=CaSO3°˝+2HClO
°° °°D£ÆœÚ‰ÂªØ—«Ã˙»Ð“∫÷–Õ®»Îπ˝¡ø¬»∆¯£∫Fe2+ + 2Br- + 2Cl2 == Fe3+ + Br2 + 4Cl-
11£Æœ¬¡–∏˜◊È¿Î◊”£¨‘⁄÷∏∂®µƒª∑æ≥÷–“ª∂®ƒÐ¥Û¡øπ≤¥Êµƒ «
A£Æ‘⁄pHŒ™7µƒ»Ð“∫÷–£∫Ag+°¢K+°¢SO42-°¢Cl-
B£Æ‘⁄ƒÐ πpH ‘÷Ω±‰…Ó¿∂…´µƒ»Ð“∫÷–£∫Na+°¢S2-°¢NO3-°¢CO32-
C£Æ‘⁄º”»Î¬¡∑€ƒÐ≤˙…˙H2µƒ»Ð“∫÷–£∫NH4+°¢Fe2+°¢SO42-°¢NO3-°¢
D£Æ‘⁄”…ÀƵÁ¿Î≥ˆµƒc(OH-)=10-13mol°§L-1µƒ»Ð“∫÷–£∫Na+°¢Fe3+°¢Cl-°¢I-
10£Æ”–πÿœ¬¡– ‘º¡µƒ±£¥Ê∑Ω∑®’˝»∑µƒ «(°°°° )
¢ŸNaOHπÃñ£¥Ê‘⁄≈‰”–œ∆§»˚µƒœ∏ø⁄∆ø÷–£ª
¢⁄Na2CO3»Ð“∫Õ®≥£±£¥Ê‘⁄≈‰”–œ∆§»˚µƒœ∏ø⁄∆ø÷–£ª
¢€“∫‰ÂÕ®≥£”√ÀÆ∑‚±£¥Ê£ª°°°°°°°°°° ¢ÐÔƱ£¥Ê‘⁄√∫”Õ÷–£ª
¢ð≈®œıÀ·Õ®≥£±£¥Ê‘⁄◊ÿ…´œ∏ø⁄∆ø÷–°£
A£Æ¢Ÿ¢€¢ð°°°° °°°°°°°°°° B£Æ¢⁄¢€¢ð°°°°°° °°°°°°°° C£Æ¢⁄¢Ð¢ð°° °°°°°°°° °°D£Æ¢Ÿ¢€¢Ð
9£Æ2008ƒÍ9‘¬25»’£¨‘ÿ”–»˝√˚∫ΩÃÏ‘±µƒ…Ò÷ð∆þ∫≈‘⁄æ∆»™∑¢…‰÷––ƒÀ≥¿˚…˝ø’£¨”Ó∫Ω‘±≥ˆ≤’ªÓ∂Ø≤¢∞≤»´∑µªÿ£¨Œ“π˙µƒ‘ÿ»À∫ΩÃÏ ¬“µ”÷»°µ√–¬µƒÕª∆∆°£°°Õ∆∂Ø…œ«ß∂÷ªº˝∫Õ∑…¥¨µƒæޥۃСø «¥”ƒƒ¿Ô¿¥µƒ£øªº˝ π”√µƒ»º¡œ «∆´∂˛º◊ά[(CH3)2NNH2]£¨ªº˝…˝ø’ ±∑¢…˙µƒªØ—ß∑¥”¶Œ™£∫C2H8N2+2N2O4£Ω2CO2°¸+3N2°¸+4H2O°¸œ¬¡–”–πÿ∏√∑¥”¶µƒÀµ∑®’˝»∑µƒ «(°°°° )
A£Æ∏√∑¥”¶µƒ—ıªØº¡ «∆´∂˛º◊ά°°°°°° °°B£Æ∏√∑¥”¶Ω¯–– ±∞—»»ƒÐ◊™±‰≥…ªØ—߃Ð
C£Æ∏√∑¥”¶÷–µ™‘™ÀÿµƒªØ∫œº€…˝∏þ°°°° °°D£Æ∏√∑¥”¶÷–√ø…˙≥…1molCO2◊™“∆8molµÁ◊”
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com