
5.用下列实验装置进行的实验中,能达到相应实验目的的是 ( )
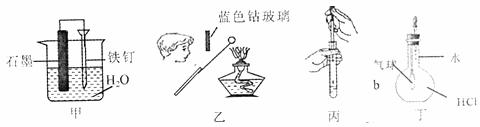
A.装置甲:防止铁钉生锈 B.装置乙:检验CaCl2中的Ca2+
C.装置丙:向试管中滴加液体 D.装置丁:验证HCl气体在水中的溶解性
4.下列物质之间的转化能用“甲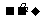 乙
乙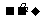 丙
丙 →丁”的形式表示是( )
→丁”的形式表示是( )
①Na→NaOH ②Cu→Cu(H)2 ③H2S→H2SO3 ④CH3OH→HCOOCH3
A.①③ B.②④ C.①②④ D.①③④
3.含杂质M(不超过0.5g)的金属锌6g,和足量的稀硫酸反应,生成0.2g氢气,则M可能是 ( )
A.K B.Mg C.Cu D.Fe
2.下列表示物质结构的化学用语或模型图正确的是 ( )
A.HClO的结构式:H-O-Cl B.H2O2的电子式: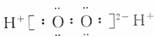
C.CO2原比例模型: D.14C的原子结构示意图:
D.14C的原子结构示意图:
1.下列叙述不正确的是 ( )
A.北京奥运“祥云”火炬的燃料丙烷是化合物
B.用于建设北京奥运主场馆“鸟巢”的钢是纯净物
C.发射“嫦娥”卫星的火箭推进剂中的四氧化二氮是氧化物
D.抗冰雪灾害时使用的融雪剂所含的氯化钠、氯化镁、氯化钙属于盐
28.(8分)实验室里常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为: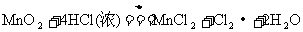 ,请回答下列问题:
,请回答下列问题:
(1)反应物中,氧化剂是____________,化合价升高的元素是____________;
(2)取一定体积的浓盐酸与MnO2发生反应,产生的氯气在标准状况下的体积为1.12L(忽略Cl2的溶解)。则参加反应的HCl的物质的量是____________,反应中被氧化的HCl的质量是____________;反应中转移的电子____________个;
(3)实验所用的浓盐酸质量分数为36.5%,密度为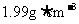 ,为了使用方便,请你计算出该浓盐酸的物质的量浓度(写出计算过程)。
,为了使用方便,请你计算出该浓盐酸的物质的量浓度(写出计算过程)。
27.(4分),一定量的液态化合物XY2,在一定量O2中恰好完全反应:
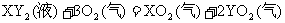
冷却后在标准状况下,测得生成物的体积为672mL,密度为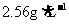 。则:
。则:
(1)反应前O2在标准状况下的体积是____________mL;
(2)化合物XY2的摩尔质量是____________。
26.(8分)实验室要配制250mL 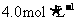 的氯化钠溶液。请回答下列问题:
的氯化钠溶液。请回答下列问题:
(1)应用托盘天平称取NaCl固体____________g;
(2)下列仪器中,配制时可能不会用到的是(填字母)____________;
A.锥形瓶 B.100mL容量瓶
C.胶头滴管 D.25mL容量瓶
(3)除上述(2)中用到的仪器外,还缺少的玻璃仪器是________________________;
(4)某同学观察液面的情况如下图所示,对所配溶液浓度有何影响?____________(填“偏高”、“偏低”或“无影响”);
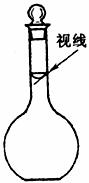
(5)某同学在配制过程中,不慎使凹液面最低点超过了容量瓶的刻度线,请你用简要的文字写出处理的方法_______________________________________________。
25.(4分)请你运用所学的知识,设计一个最简单可行的实验,证明钠的熔点低、密度比水小。根据你的设计填写下列空白:
(1)实验过程简述________________________________________________;
(2)密度比水小的现象_______________________________________________;
(3)熔点低的现象____________________________________________________;
(4)有关的化学方程式________________________________________________。
24.(10分)据下图的转化关系及现象回答下列问题。
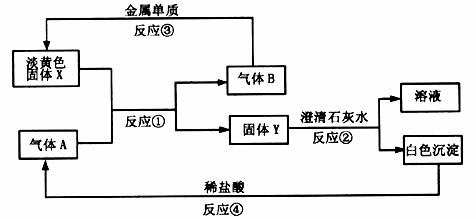
(1)固体X的名称________________,气体A的化学式________________;
(2)写出反应①③的化学方程式:
①________________________________________________;
③________________________________________________;
(3)写出反应②④的离子方程式
②________________________________________________;
④________________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com