
10ĢŪŌŅÖŠÐŋž°ÆäŧŊšÏÎïĩÄÐÔÖĘÓëÂÁž°ÆäŧŊšÏÎïÏāËÆĄĢČįÍžĢŽšáŨøąęΊČÜŌšĩÄpHĢŽŨÝŨøąęΊZn2+ĀëŨÓŧō[Zn(OH)4]2ÔĀëŨÓĩÄÎïÖĘĩÄÁŋÅĻķČ(žŲÉčZn2+ĀëŨÓÅĻķČΊ10-5molĄĪL-1 ĘąĢŽZn2+ĀëŨÓŌŅģÁĩíÍęČŦ)ĄĢÏÂÁÐËĩ·ĻēŧÕýČ·ĩÄĘĮ (ĄĄĄĄ )
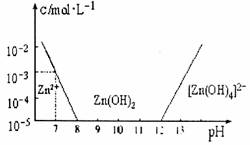
ĄĄĄĄĄĄ AĢŪÍųZnC12 ČÜŌšÖОÓČëŨãÁŋĩÄNaOH ČÜŌšĢŽ·īÓĶĩÄĀëŨÓ·―ģĖĘ―ŋÉąíĘūΊĢš
Zn2+ +4OH-= [Zn(OH)4]2-
ĄĄĄĄĄĄ BĢŪģýČĨÃū·ÛÖÐĩÄÔÓÖĘÐŋ·ÛĢŽŋÉŌÔžÓČëŨãÁŋĩÄNaOH ČÜŌšĢŽđýÂËĢŽÏīĩÓĢŽļÉÔï
ĄĄĄĄĄĄ CĢŪÄģ·ÏŌšÖКŽZn2+ĀëŨÓĢŽģÁĩíZn2+ĀëŨÓŋÉŌÔŋØÖÆČÜŌšpHĩÄ·ķΧĘĮ8-12
ĄĄĄĄĄĄ DĢŪÏō1 L 1 molĄĪL-1ĩÄZnC12 ČÜŌšÖОÓČëNaOH đĖĖåÖÁpH=7ĢŽÐčNaOH 2 mol
9ĢŪÏÂÁÐĘĩŅé·―·ĻŧōēŲŨũšÏĀíĩÄĘĮĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄ (ĄĄĄĄ )
ĄĄĄĄĄĄ AĢŪÓÃÆ·šėČÜŌšžøąðŌŌČĐĄĒą―ĄĒÏõŧųą―
ĄĄĄĄĄĄ BĢŪÓÃ10mLÁŋÍēŨžČ·ÁŋČĄ8. 00mL ĄĄ1mol/L ĩÄKMnO4 ČÜŌš
ĄĄĄĄĄĄ CĢŪģýČĨą―ÖÐĩÄÉŲÁŋą―·ÓĢŽŋÉžÓČëÅĻäåËŪšóđýÂË
ĄĄĄĄĄĄ DĢŪΊŨžČ·ēâķĻŅÎËáÓëNaOH ČÜŌš·īÓĶĩÄÖКÍČČĢŽËųÓÃËášÍžîĩÄÎïÖĘĩÄÁŋÏāĩČ
8ĢŪÔÚ(NH4)2Fe(SO4)2ĄĪ6H2O ū§ĖåČÜÓÚËŪšóĩÄČÜŌšÖÐĢŽžÓČëÏÂÁÐÎïÖĘēŧÄÜ·ĒÉú·īÓĶĩÄĘĮ(ĄĄĄĄ )
ĄĄĄĄĄĄ AĢŪHNO3 ĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄ BĢŪHCl ĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄ CĢŪNaOH ĄĄĄĄĄĄĄĄĄĄĄĄĄĄ DĢŪCl2
7ĢŪ°Ē·üžÓĩÂÂÞģĢĘýÓÃNAąíĘūĢŽÔōÏÂÁÐÐðĘöÖÐÕýČ·ĩÄĘĮ
ĄĄĄĄĄĄ AĢŪ0.1molMgÔÚŋÕÆøÖÐÍęČŦČžÉÕĢŽÉúģÉMgOšÍMg3N2ĢŽŨŠŌÆĩįŨÓĘýĘĮ0ĢŪ2NA
ĄĄĄĄĄĄ BĢŪ0.1 mol ĖúÔÚ0ĢŪ1 mol Cl2 ÖÐģä·ÖČžÉÕĢŽÓÐ0.3NAļöĩįŨÓŨŠŌÆ
ĄĄĄĄĄĄ CĢŪ1molļĘ°ąËá·ÖŨÓÖÐīæÔÚ9NAķÔđēÓÃĩįŨÓ
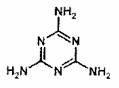
ĄĄĄĄĄĄ DĢŪ0.1molČýūÛĮč°·(―áđđĘ―ČįÉÏÍž)šŽ0. 3NAļöC=N ËŦžü
6ĢŪČËÃĮÉúīæĩÄŧ·ūģÓëŧŊŅ§ÏĒÏĒÏāđØĢŽÏÂÁÐËĩ·ĻÖÐĢŽÄãČÏΊÕýČ·ĩÄĘĮ
ĄĄĄĄĄĄ AĢŪÆûģĩÎēÆøÖКŽÓÐÄÜÎÛČūŋÕÆøĩÄĩŠĩÄŅõŧŊÎïĢŽÔŌōĘĮÆûÓÍČžÉÕēŧģä·Ö
BĢŪÖīÐÐĄ°ÏÞËÜÁÖũŌŠĘĮΊÁË―ÚÔžÄÜÔī
CĢŪĮåģŋĢŽČÕģöšóĩÄÃÜÁÖÖÐŋÉŋīĩ―ÂÆÂÆđâĘøĢŽÔŌōĘĮĮåģŋÁÖžäCO2ĩÄÅĻķČ―Ïīó
DĢŪļÖĖúÔÚģąĘŠĩÄŋÕÆøÖÐļüŌŨÉúÐâĢŽĘĮŌōΊÐÎģÉÁËÔĩįģØĩÄÔĩđĘ
23ĢŪČËÃĮÉúŧîÖÐĘđÓÃĩÄŧŊÏËĩØĖšĄĒČýšÏ°åĄĒÓÍÆáĩČŧŊđĪēúÆ·ĢŽŧáĘÍ·ÅģöÄģÖÖÎÛČūŋÕÆøĩÄÆøĖåAĄĢΊĘđŌ·þīïĩ―·ĀÖåĄĒļÄÉÆĘÖļÐĩČЧđûĢŽÔÚÖÆŨũđýģĖÖÐŌēĖížÓAĄĢĩŦŌ·þÖÐēÐÁôĩÄAģŽąęŧáÎĢšĶČËĖå―ĄŋĩĄĢAĩÄŧŊŅ§Ę―Ί___________ĢŽĘĮŌŧÖÖ___________ÉŦĄĒÓÐīĖžĪÐÔÆøÎķĢŽ___________ČÜÓÚËŪĢŽ___________ķūĩÄÆøĖåĢŧÐÂÂōĩÄŌ·þČôÓÐīĖžĪÐÔÆøÎķĢŽÓÐŋÉÄÜĘĮAšŽÁŋģŽąęĢŽËųŌÔĢŽÂōŧØ·þŨ°šóÓĶÏČÓÃËŪÏīĢŽŌÔČĨĩôēÐÁôĩÄAĄĢ
22ĢŪ(9·Ö)ĩ°°ŨÖĘĘĮÉúÎïĖåÄÚĩÄÖũŌŠÉúÃüÎïÖĘĢŽÆäÏāķÔ·ÖŨÓÖĘÁŋūÞīóĢŽÖÖĀā·ąķāĢŽ―áđđŌē·ĮģĢļīÔÓĄĢĩ°°ŨÖĘËųšŽĩÄÔŠËØÖÁÉŲÓÐ__________ĄĒ__________ĄĒ__________ĄĒ__________ĢŽĖėČŧĩ°°ŨÖĘËŪ―âĩÄēúÎïĘĮ___________ĢŽļĘ°ąËáĩÄ―áđđžōĘ―ĘĮ___________ĢŽĮø·ÖīŋÃŦÏßÓëŧŊÏËÃŦÏßĩÄ·―·ĻĘĮ_________________________________ĄĢ
21ĢŪÏÂąíĘĮÄģĘģÆ·°üŨ°īüÉÏĩÄËĩÃũĄĢ
|
Æ·Ãû |
ĄÁĄÁĄÁĄÁĄÁĄÁ |
|
ÅäÁÏ |
ÏĘžĶĩ°ĄĒūŦÃæ·ÛĄĒ°ŨÉ°ĖĮĄĒūŦÁķÖēÎïÓÍĄĒÄĖÓÍĄĒÄĖ·ÛĄĒĖžËáĮâÄÆĄĒÄûÃĘÖĄĒĘģŅÎĩČ |
|
ąĢÖĘÆÚ |
240Ėė |
|
ÉúēúČÕÆÚ |
žû·âŋÚ |
īÓąíÖÐĩÄÅäÁÏÖÐ·ÖąðŅĄģöŌŧÖÖÎïÖĘĖîÔÚÏāÓĶĩÄšáÏßÉÏĄĢ
(1)ļŧšŽĩ°°ŨÖĘĩÄĘĮ___________ĢŧĄĄĄĄĄĄ (2)ļŧšŽĖĮĀāĩÄĘĮ___________Ģŧ
(3)ļŧšŽÓÍÖŽĩÄĘĮ___________ĢŧĄĄĄĄĄĄĄĄĄĄ (4)ļŧšŽÎŽÉúËØĩÄĘĮ___________Ģŧ
20ĢŪ(6·Ö)ÄģŋđËáŌĐĩÄÖũŌŠģÉ·ÝÓÐĖĮŌÂĄĒĮâŅõŧŊÂÁĄĒĩí·ÛĄĢ
(1)ļÃŋđËáŌĐĩÄÓÐЧģÉ·ÝĘĮ___________Ģŧ
(2)ÐīģöļÃŋđËáŌĐ·ĒŧÓđĶÐ§ĘąĩÄĀëŨÓ·―ģĖĘ―_________________________________ĄĢ
(3)ČôīËŋđËáŌĐÃŋÆŽšŽĮâŅõŧŊÂÁ195mgĢŽČĄŌŧÆŽÕâÖÖŌĐÆŽÄëËéšóÓëŨãÁŋĩÄŅÎËá·īÓĶĢŽđēÏûšÄŅÎËáÖÐČÜÖĘĩÄÎïÖĘĩÄÁŋĘĮ___________molĄĢ
19ĢŪ(8·Ö)AĘĮŌŧÖÖ°ŨÉŦū§ĖåĢŽĘÜČČ·Ö―âÄÜÉúģÉBĄĒCÁ―ÖÖÎÞÉŦÆøĖåĢŽCĩÄËŪČÜŌšÓëÏõËáŌøČÜŌš·īÓĶēúÉú°ŨÉŦģÁĩíĄĢAÓëÅĻNaOHČÜŌšđēČČĢŽ·ÅģöÎÞÉŦÆøĖåBĄĢČôÔÚÔēĩŨÉÕÆŋÖÐ·ÖąðĘÕžŊļÉÔïĩÄÆøĖåBšÍCĢŽČŧšó―ŦĘÕžŊÂúÆøĖåĩÄÉÕÆŋ°īČįÍžËųĘūŨ°ÖÃŨéŨ°ĢŽž·ŅđĩÎđÜĩÄ―šÍ·ĘąĢŽŋÉŌÔ·ÖąðĩÃĩ―ĀķÉŦÅįČŠšÍšėÉŦÅįČŠĄĢĮëĖîÐīÏÂÁÐŋÕ°ŨĢš
(1)AĩÄŧŊŅ§Ę―ĘĮ___________Ģŧ
(2)ĘÕžŊÆøĖåBĩÄ·―·ĻĘĮ______________________Ģŧ
(3)BÓëCÁ―ÆøĖåÏāÓöĘąĢŽŋÉđÛēėĩ―ĩÄÏÖÏóĘĮ_________________________________Ģŧ
(4)AÓëÅĻNaOHČÜŌšđēČČĘąĢŽ·ĒÉú·īÓĶĩÄĀëŨÓ·―ģĖĘ―ĘĮ______________________ĄĢ
đúžĘŅ§ÐĢÓÅŅĄ - Á·Ï°ēáÁÐąí - ĘÔĖâÁÐąí
šþąąĘĄŧĨÁŠÍøÎĨ·ĻšÍēŧÁžÐÅÏĒūŲąĻÆ―ĖĻ | ÍøÉÏÓКĶÐÅÏĒūŲąĻŨĻĮø | ĩįÐÅÕĐÆūŲąĻŨĻĮø | ÉæĀúĘ·ÐéÎÞÖũŌåÓКĶÐÅÏĒūŲąĻŨĻĮø | ÉæÆóĮÖČĻūŲąĻŨĻĮø
ÎĨ·ĻšÍēŧÁžÐÅÏĒūŲąĻĩįŧ°Ģš027-86699610 ūŲąĻÓĘÏäĢš58377363@163.com