
17.将H2(g)和Br2(g)充入恒容密闭容器,恒温下发生反应H2(g)+Br2(g)
 2HBr(g)
2HBr(g)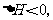 g平衡时Br2(g)的转化率为a;若初始条件相同,绝热(密闭容器与环境无能量交换)下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是
g平衡时Br2(g)的转化率为a;若初始条件相同,绝热(密闭容器与环境无能量交换)下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是
A.a>b B.a=b C.a<b D.无法确定
16.下图为阳离子交换膜法电解饱和食盐水原理示意图。下列说法不正确的是
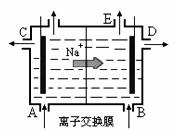
A.从E口逸出的气体是H2
B.从B口加入含少量NaOH的水溶液以增强导电性
C.标准状况下每生成22.4 LCl2,便产生2 mol NaOH
D.粗盐水中含Ca2+、Mg2+、Fe3+、SO42-等离子,精制时先加Na2CO3溶液
15.电解100mL含 c(H+)=0.30mol/L的下列溶液,当电路中通过0.04mol电子时,理论上析出金属质量最大的是
A.0.10mol/LAg+ B.0.02mol/L Zn2+
C.0.20mol/L Cu2+ D.0.20mol/L Pb2+
14.下列叙述正确的是
①锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率。
②镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀。
③电镀时应把镀件置于电解槽的阴极。
④冶炼铝时,把氧化铝加入液态冰晶石中成为熔融体后电解。
⑤钢铁表面常易腐蚀生成Fe2O3·nH2O
A.①②③④⑤ B.①③④⑤ C.①③⑤ D.②④
13.在0.1mol/LNaHSO3溶液中存在着微粒浓度的关系式,正确的是
A.C(Na+) > C(HSO3-) > C(SO32-) > C(H+) > C(OH-)
B.C(Na+) + C(H+) = C(HSO3-) + C(SO32-) + C(OH-)
C.C(Na+) + C(H+) < C(HSO3-) + C(SO32-) + C(OH-)
D.C(Na+) = C(HSO3-) + C(SO32-) + C(H2SO3)
12. 在由水电离出C(H+)=1×10-13 mol·L-1的溶液中,一定不能大量共存的离子组是
A.Cl― AlO2― Na+ K+ B.Fe3+ NO3― MnO4― K+
C.Fe2+ NO3― Ba2+ Cl― D.CO32― Na+ Cl― K+
11. 下列分离或提纯物质的方法错误的是
A.用渗析的方法精制氢氧化铁胶体
B.用加热的方法提纯含有少量碳酸氢钠的碳酸钠
C.用溶解、过滤的方法提纯含有少量硫酸钡的碳酸钡
D.用盐析的方法分离、提纯蛋白质
10.用已知浓度的盐酸滴定用NaOH固体配成的碱溶液时,下列操作使滴定结果偏高的是
A.NaOH固体称量时间过长
B.盛标准盐酸的滴定管用碱液润洗
C.用酚酞做指示剂
D.固体NaOH中含KOH
9.如下图所示的烧杯中盛的是天然水,铁的腐蚀速度由快到慢的顺序是
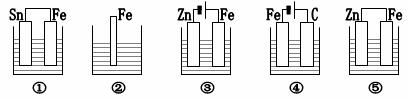
A.⑤①②③④ B.③①②⑤④ C.⑤①③④② D.③④⑤①②
8.镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O Cd(OH)2 + 2Ni(OH)2
Cd(OH)2 + 2Ni(OH)2
有关该电池的说法正确的是
A.充电时阳极反应:Ni(OH)2-e-+OH―== NiOOH + H2O
B.充电过程是化学能转化为电能的过程
C.放电时负极附近溶液的碱性不变
D.放电时电解质溶液中的OH―向正极移动
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com