
15.将0.2 mol/L NaA溶液和0.1 mol/L盐酸等体积混合后,溶液pH>7,则以下关系式错误的是 ( )
A.c(A-)> c(HA)
B.c(HA)+c(A-)=0.1mol/L
C.c(Na+)+c(H+)= c(A-)+c(Cl-)+c(OH-)
D.c(Na+)= c(A-)+ c(HA)
14.实验室制取少量FeO,以下方法中能得到FeO是 ( )

13.以水为溶剂进行中和滴定的原理是:H3O++OH-=2H2O。已知液态SO2和纯水的导电性相近,因为液态SO2也会发生自离解: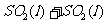

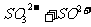 。若以液态SO2为溶剂,用SOCl2滴定Cs2SO3,则以下叙述错误的是 (
)
。若以液态SO2为溶剂,用SOCl2滴定Cs2SO3,则以下叙述错误的是 (
)
A.该滴定反应可以表示为:SO32- + SO2+ = 2SO2
B.在一定温度下,液态SO2中c(SO32-)与c(SO2+)的乘积是一个常数
C.自离解的存在,说明SO2是离子化合物
D.可通过导电能力变化来判断是否到达滴定终点
12.电解NaCl-KCl-AlCl3熔融体来制取金属铝比电解Al2O3-Na3AlF6熔融体节省电能30%,但现在仍用后一种方法制取铝,最主要的理由是 ( )
A.自然界铝元素主要以Al2O3形式存在
B.前一种方法会产生有毒气体
C.后一种方法还可以制得氧气
D.Na3AlF6比NaCl、KCl价格更低廉
11.肼(N2H4)是火箭发动机的燃料,反应时N2O4为氧化剂,生成氮气和水蒸气。已知:
N2(g)+2O2(g)=N2O4(g);△H=+8.7kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-534.0kJ/mol
下列表示肼跟N2O4反应的热化学方程式,正确的是 ( )
A.2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g);△H=-542.7kJ/mol
B.2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g);△H=-1059.3kJ/mol
C.2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g);△H=-1076.7kJ/mol
D.N2H4(g)+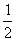 N2O4(g)=
N2O4(g)=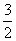 N2(g)+2H2O(g);△H=-1076.7kJ/mol
N2(g)+2H2O(g);△H=-1076.7kJ/mol
10.为确定某溶液的离子组成,进行如下实验:
①测定溶液的pH,溶液显强碱性。
②取少量溶液加入稀盐酸至溶液呈酸性,产生无刺激性、能使澄清石灰水变浑浊的气体。
③在上述溶液中再滴加Ba(NO3)2溶液,产生白色沉淀。
④取上层清液继续滴加Ba(NO3)2溶液至无沉淀时,再滴加Ag NO3溶液,产生白色沉淀。
根据实验以下推测正确的是 ( )
A.一定有SO32-离子 B.一定有CO32-离子
C.一定有C1-离子 D.不能确定HCO3-离子是否存在
9.某研究性学习小组为了探索镁粉与溴水反应的机理,做了如下四组实验
①将镁粉投入冷水中,未见任何现象;
②将镁粉放入溴水中,观察到只是开始时产生极少量的气泡,但溴水的颜色逐渐褪去;
③将镁粉放入液溴中,未观察到任何明显现象;
④向含足量镁粉的液溴中滴加几滴水,观察到溴的红棕色很快褪去。
则下列关于镁与溴水的反应机理的论述中正确的是 ( )
A.镁粉只直接与溴水中的溴反应
B.镁粉只与溴水中的酸反应
C.产生极少量的气泡是由于镁粉与水反应得到
D.镁粉在水的催化下与溴发生反应
8.下列离子方程式中正确的是: ( )
A.向碳酸氢钙溶液中加入过量氢氧化钠
Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32-
B.氧化铁可溶于氢碘酸:Fe2O3+6H+=2Fe3++3H2O
C.Fe3+的检验:Fe3++3SCN-=Fe(SCN)3↓
D.Na2S溶液呈碱性:S2-+H2O=HS-+OH-
7.在加入铝粉能放出H2的溶液中,可能大量共存的是 ( )
A.NH4+、NO3-、CO32-、Na+ B.Na+、Ba2+、Mg2+、HCO3-
C.NO3-、K+、SO42-、Cl- D.NO3-、Na+、Fe2+、K+
6.下列在一定条件下进行的反应属于水解反应的是 ( )
① C12H22O11(麦芽糖) + H2O→2C6H12O6 ② CH2=CH2 + H2O →C2H5OH
③ CH3CH2Cl + H2O→ CH3CH2OH + HCl ④ NH3·H2O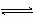 NH4+ + OH-
NH4+ + OH-
⑤ CH3CH2ONa + H2O→ CH3CH2OH + NaOH ⑥ CaC2 + 2H2O→Ca(OH)2 + C2H2↑
A.②④ B.①②⑤ C.③④⑥ D.①③⑤⑥
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com