
6.已知化学反应C(s)+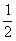 O2(g)==CO(g);⊿H=-Q1kJ·mol-1,2CO(g)+ O2(g)==2CO2(g);⊿H=-Q2kJ·mol-1,据此推断,下列说法正确的是(Q、Q均为正数,且其他条件相同) ( )
O2(g)==CO(g);⊿H=-Q1kJ·mol-1,2CO(g)+ O2(g)==2CO2(g);⊿H=-Q2kJ·mol-1,据此推断,下列说法正确的是(Q、Q均为正数,且其他条件相同) ( )
A.碳的燃烧热为Q1kJ·mol-1
B.2 molCO(g)所具有的能量一定高于2 molCO2(g)所具有的能量
C.一定质量的碳燃烧,生成CO2(g)比生成CO(g)时放出的热量多
D.碳燃烧生成CO2气体的热化学方程式为C(s)+O2(g)==CO2(g);⊿H=-(Q1+Q2)kJ·mol-1
5.下列溶液中,各组离子可能大量共存的是 ( )
A.pH=1的溶液中:K+、Fe2+、Cl-、NO3-
B.在强酸性溶液中:Cu2+、ClO-、Cl-、Ba2+
C.在含有大量Fe3+的溶液中:NH4+、Cl-、Na+、AlO2-
D.由水电离的c(H+)=10-13 mol·L-1的溶液中:Al3+、K+、NO3-、SO42-
4.2007年7余额2日,美、德两国成功合成具有化学特性的氢铝化合物(AlH3)n,关于氢铝化合物的推测不正确的是 ( )
A.氢铝化合物与水反应生成氢氧化铝和氢气
B.氢铝化合物中铝显+3价,H显-1价
C.铝与水蒸汽高温下反应生成氢铝化合物
D.氢铝化合物具有强还原性
3.化学与生产、生活、社会密切相关。下列有关说法中不正确的是 ( )
A.2008年北京奥运会开幕式上的“脚印等焰火让全世界为之欢呼、倾倒,这主要是利用了化学中“颜色反应”的有关知识
B.神七宇航员所穿航天服是由我国自行研制的新型“连续纤维增韧”航空材料做成,其主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它是一种新型无机非金属材料
C.三鹿婴奶粉中的三聚氰胺的结构如右图所示: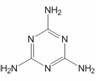 则其化学式为C3N6H6
,
则其化学式为C3N6H6
,
D.蛋白质都是由氨基酸形成的不可降解的高分子化合物,其水溶液有丁达尔现象
2.“假说”在化学科学的研究和发展中起着重要的作用。下列“假说”在化学科学发展过程中曾经起到一定的作用,从目前的化学理论看,仍然合理的是 ( )
A.道尔顿提出的“每一元素的原子以其原子质量为其特征,原子是不可分的”
B.阿伦尼乌斯提出的“电解质在水溶液中能离解成带电的粒子”
C.贝彩里乌斯提出的“不同原子带不同的电性,因而产生吸引力,由此形成化合物”
D.盖•吕萨克提出的“在同温同压下,相同体积的不同气体含有相同数目的原子”
1.分类是学习和研究化学的一种常用的科学方法。下列分类合理的是 ( )
①根据酸分子中含有的H原子个数将酸分为一元酸、二元酸等
②根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应
③根据电解质在熔融状态下能否完全电离将电解质分为强电解质和弱电解质
④根据元素原子最外层电子数的多少将元素分为金属和非金属
⑤根据反应的热效应将化学反应分为放热反应和吸热反应
A.②③ B.①②④ C.②⑤ D.②③④⑤
33.(8分)[有机化学基础]
在下图所示的转化关系中。A是一种链状羧酸,分子式为C3H4O2;F中含有七个原子构成的环;H是一种高分子化合物。请填写下列空白:
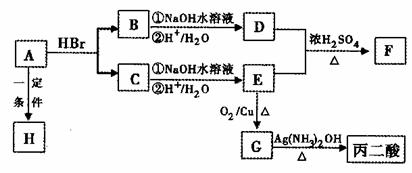
(1)写出F的结构简式:
(2)请写出:
①A→H的化学方程式:
②B与NaOH溶液反应的化学方程式:
(3)反应G→丙二酸的反应类型是:
32.(8分)[物质结构与性质]
现有部分前四周期元素的性质或原子结构如下表:
|
元素编号 |
元素性质或原子结构 |
|
A |
第三周期中的半导体材料 |
|
B |
L层s电子数比p电子数少l |
|
C |
第三周期主族元素中其第一电离能最大 |
|
D |
前四周期元素中其未成对电子数最多 |
(1)B单质分子中,含有 个σ键和 个π键,元素B的气态氢化物的空间构型为 。
(2)C单质的熔点 A单质的熔点(填“高于”或“低于”),其原因是:
(3)写出元素D基态原子的电子排布式: 。
31.(8分)[化学与技术]
海洋约占地球表面积的71%,是一个远未完全开发的巨大化学资源宝库,海水水资源的利用和海水化学资源的利用具有非常广阔的前景。
从海水中可以获取食盐、镁、钾、溴及其化工产品。空气吹出法是目前从海水中提取澳的常用方法,具体流程如下:
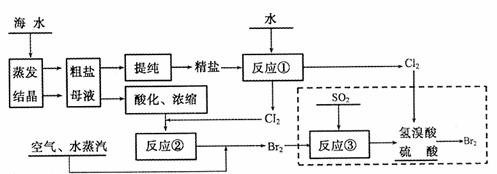
请回答:
①实验室中粗盐提纯的过程中添加的试剂及顺序: ;
在反应②得到的溶液中通人空气、水蒸汽的作用是 ;
②反应①、反应③的离子方程式分别为 、 ;
③上述流程中虚线方框内生产流程的作用是 。
30.(12分)某校化学研究小组的同学已知碳酸钠和碳酸氢钠的化学性质,并对碳酸钠和碳酸氢钠的活泼性进行了如下实验探究:
I.为了鉴别碳酸钠和碳酸氢钠两种白色固体,小组成员用不同的方法进行了实验,如 下图装置所示:
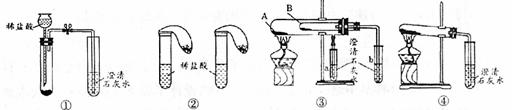
(1)只根据图①、图②所示实验,能够明确达到实验目的的是 (填“①”或“②”)
(2)若用图③所示实验装置验证碳酸钠比碳酸氢钠的稳定性好,则碳酸氢钠应装入
管中(填“A”或“B”)。
(3)有同学提出用图④所示实验装置就能在一次实验、一个反应中比较出碳酸钠和碳酸氢钠的热稳定性相对强弱,你认为这个说法 (填“正确”或“不正确”)
II.已知:10℃时,在烧杯中加入0.1mol/L的NaHCO3溶液400mL,测得该溶液在不同温度下的pH(见下表):
|
温度(℃) |
10 |
20 |
30 |
50 |
|
pH |
8.3 |
8.4 |
8.5 |
8.9 |
甲同学将200mL、20℃、0.lmol/L的NaHCO3溶液置于烧杯中加热至50℃,测其pH为8.9;再将溶液冷却至20%,测其pH仍为8.4。乙同学将200mL、20℃、0.1mol/L的NaHCO3溶液置于烧杯中加热至90%一段时间后,将溶液冷却至20℃,测其pH为10.1(溶液体积不变)。
请对上述实验现象作出说明。
[选做部分]
共8个题,考生从中选择2个物理题、1个化学题和1个生物题作答
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com